2. 西安航天动力试验技术研究所, 陕西, 西安 710100;
3. 西北工业大学动力与能源学院, 陕西 西安 710072;
4. 中国工程物理研究院化工材料研究所, 四川 绵阳 621999
2. Xi′an Aerospace Propulsion Institute, Xi′an 710100, China;
3. School of Power and Energy, Northwestern Polytechnical University, Xi′an 710072, China;
4. Institute of Chemical Materials, CAEP, Mianyang 621999, China
自燃型液体推进剂是指在火箭发动机使用条件下液体氧化剂和液体燃料相互接触后能自燃的双组元液体推进剂[1]。这一推进剂具有多种优点, 如无需外界点火源, 推进器装置更为简便安全, 具有较高比冲, 可以通过调节燃料流量实现推力大小的控制, 作业中可以多次点火启动等。因此, 自燃型液体推进剂可广泛应用于弹道导弹和大多数航天器, 包括载人飞行器, 行星探测器和卫星。目前, 自燃型液体推进剂普遍采用肼类燃料及其衍生物, 这类燃料不仅储存和运输成本高, 还具有高挥发性、毒性和致癌性[1], 因此, 近年来国内外广泛开展了肼类燃料替代推进剂的研究[2-7]。其中, 高能离子液体作为一种无污染的液体自燃推进剂引起科研界的广泛重视。离子液体是由有机阳离子和无机阴离子或有机阴离子组成的低温熔融盐, 其本身具有不挥发性和低毒性, 使其在作为推进剂燃料时非常安全, 便于运输、存储和实际操作[8]。
目前, 国内外许多研究小组在离子液体合成方面做出了突出贡献[9-11], 但是在离子液体和氧化剂的反应过程和自着火机理方面的研究十分匮乏。2008年, 普渡大学的Schneider等[12]首次报道了关于二氰胺类离子液体推进剂, 指出具有富燃性和低粘度的二氰胺类离子液体可与白烟硝酸或红烟硝酸发生自燃反应。然而, 该研究提供的图像不足以显示离子液体和氧化剂反应的微观现象, 不足以阐明其反应机理。最近, Sun[13]等人研究了9种二氰胺基咪唑类盐含能离子液体的阳离子结构对于自着火的影响。他们发现阳离子的结构可以影响离子液体的粘度、密度和能量性能, 这些物理性质又进一步影响了离子液体的点火过程和延迟时间。例如低粘度可以降低着火延迟时间。不足的是, 实验中用到的二氰胺类离子液体的点火延迟时间最短为25 ms, 最长超过100 ms, 这可能会造成实际推进剂应用中的硬启动问题[5]。
近期, 中国工程物理研究院的张庆华等[11]合成了8种具有相同[BH3(CN)BH2(CN)]-阴离子的新型离子液体, 这类离子液体具有熔点低、热稳定性好、粘度低、成本效益好的优点。值得一提的是, [BH3(CN)BH2(CN)]-阴离子中, {BH3}和{BH2CN}有强还原性, 可能改善离子液体的自着火表现, 氰基作为吸电子基可以提高离子液体的水稳定性[11]。基于此, 本研究通过观察离子液体与所选氧化剂的反应过程, 判断离子液体是否可以实现稳定的自着火, 同时, 解释了燃料/氧化剂组合反应过程中的微观和宏观现象的机理, 并通过一些明确的参数(如着火延迟时间(IDT), 微爆延迟时间(EDT))对反应进行了量化。
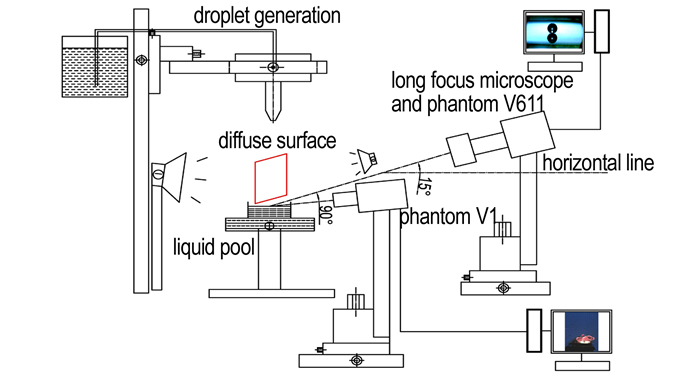
2 实验部分 2.1 实验装置与试剂离子液体自点火测量的实验系统的组成如图 1所示, 采用滴落法装置。安装在多维位移台上的1 mL用注射器配有No.26针管(外径为0.45 mm), 尖端产生直径D0大约为2.25 mm的离子液滴, 垂直地落入下方距离约为135 mm的盛有氧化剂的培养皿中, 培养皿直径为100 mm(约50D0), 深度为20 mm(约10D0)。实验用Phantom V611高速摄像机(美国VRI公司生产)配有型号为Questar QM1的长焦显微镜(德国Lavision公司生产)以15°的俯角采用7, 000 fps的帧频记录了离子液滴和氧化剂液池之间的微观现象。另一台Phantom V1高速摄像机(美国VRI公司生产)采用7, 000 fps的帧频同时记录反应的宏观现象。与V611的背光源不同, V1相机采用散射光源, 从而可以更全面地观察着火过程。
|
图 1 离子液体自点火测量的实验系统示意图 Fig.1 Sketch of the experimental system for ionic liquids hypergolic measurement |
试剂: 8种离子液体, 均含有相同的[BH3(CN)BH2(CN)]-阴离子, 其化学结构式及理化性质见表 1。两种氧化剂:白色发烟硝酸(WFNA, 97.5%HNO3, 水含量小于2%,NO2含量大于0.5%)和红色发烟硝酸(RFNA, 84%HNO3, (14±1)%NO2和1%~2%水)均购自西安航天动力研究所。
| 表 1 8种离子液体的化学结构及物理性质 Tab.1 Chemical structures and physical properties of the eight ionic liquids(I.L.s) |
实验中使用的氧化剂具有挥发性, 所有的准备工作应在通风橱中进行, 并且实验区域需要配备通风装置。在实验开始之前, 用玻璃板覆盖盛有氧化剂的培养皿以降低氧化剂蒸发对实验的影响。之后在离子液滴落下前, 及时将玻璃板移开。由于培养皿体积大, 可以容纳足够的液体氧化剂, 并且氧化剂液体体积约为离子液滴体积的15000倍, 因此几滴燃料和反应产物不会污染氧化剂液池, 所以不必在每次实验前更换氧化剂, 经过约5次滴落实验后更新氧化剂液池。
3 结果与讨论 3.1 实验现象 3.1.1 剧烈的微爆和自着火8种离子液体分别与氧化剂反应的现象类似, 以反应较为剧烈、点火延迟时间较短的I.L.8为例进行讨论, 图 2给出了由两台高速摄像机拍摄得到的I.L.8液滴与WFNA反应的现象。

|
图 2 I.L.8与WFNA滴落实验现象(a~f由长焦显微V611相机拍摄得到, g~i由V1相机拍摄得到) Fig.2 Droplet test phenomena of I.L.8 reacted with WFNA(a-f were captured by V611 camera and g-i were captured by V1 camera) |
在I.L.8离子液滴撞击WFNA液池表面后, 观察到以下过程:
(1) 液相混合、微爆过程:实验中的I.L.8液滴直径为2.32 mm, 碰池速度为1.5 m·s-1。定义当液滴到达WFNA液面的时刻为0 ms(图 2a), 从微观图像中可以看出在0.57 ms时液滴表面出现两处锥状飞溅(图 2b), 之后大量的二次液滴高速向四周飞溅, 持续了大约1 ms(图 2b~图 2d)。这一反应十分剧烈, 与普通的流体动力学完全不同。液滴与WFNA液面接触时立刻发生化学反应, 提升了局部温度和压力, 有气相产物生成的同时部分WFNA液体被汽化。随着液面下压力的升高, 离子液滴冲破束缚, 小液滴随着气体向外高速飞溅。而爆炸产生的大量二次液滴又增加了与WFNA的接触面积, 加快了液相的化学反应。
(2) 气相反应、自着火过程:在2.7 ms时(图 2e), 反应的温度提升到一定条件, 气相可燃物的浓度达到一定值时, 出现气相火焰核心, 根据文献[12]定义, 从液滴碰液池第一帧图片到出现火焰第一帧图片之间的时间为着火延迟时间。火焰迅速向外扩展, 液面上出现燃烧后产生的絮状产物(图 2f)。火焰传播的同时液面下出现一个包裹火焰的弹坑(图 2h), 这很可能是由于最初的微爆产生了向四周高速飞溅的离子液滴尖刺, 部分进入氧化剂液面以下, 经过反应出现火焰。此时液面下的压力较大, 弹坑逐渐扩大直到燃料耗尽消失。同时, 可以看到液面以上的火焰呈现出四周绿色中间亮黄色的颜色, 这与硼类氧化物的燃烧现象是一致的。火焰持续了大约164 ms。
3.1.2 飞溅、反弹和短促燃烧实验中还观察到一种特殊的未见报道的自着火过程。图 3给出了I.L.8液滴与RFNA反应的过程。

|
图 3 I.L.8与RFNA滴落实验现象(a~d由长焦显微V611相机拍摄得到, e~ l由V1相机拍摄得到) Fig.3 Droplet test phenomena of I.L.8 reacted with RFNA(a-d were captured by V611 camera and e- l were captured by V1 camera) |
在I.L.8离子液滴撞击RFNA液池表面后, 观察到以下反应过程:
(1) 液相混合、莱顿弗罗斯特效应:实验中的I.L.8液滴直径为2.33 mm, 碰池速度为1.5 m·s-1。I.L.8液滴以非浸润形式撞击到RFNA液面上, 如图 3b所示。之后出现皇冠状飞溅, 有较大的二次液滴在皇冠状边缘产生, 直到连接处断裂, 二次液滴向外飞出, 落到远离I.L.8落点的地方, 同时在离子液体的落点处形成一个弹坑, 这与文献[14]相似。在1.71 ms(图 3d)时, 观察到有少量的气体产物以及氧化剂蒸汽形成的黑色烟气。黑色烟气的产生是由于离子液滴接触氧化剂液池表面时, 界面发生化学反应并释放热量和产生部分气体产物。随着局部温度升高, RFNA被汽化, 迅速形成由气态产物和RFNA蒸气组成的蒸汽层, 即所谓的莱顿弗罗斯特蒸汽层, 并阻止了液滴与液体RFNA的进一步混合。这在文献[15]中有详细阐释。
(2) 短促燃烧现象:在65.7 ms时, 白色的球形泡沫[15]随着弹坑的回缩而跳出液面(图 3e), 但是上升高度很低。在99.6 ms时, 在离子液滴落点以外的地方出现火焰核心, 并且火焰在大约100 ms(图 3g)发展到最大, 其传播仅持续4.7 ms, 同时白色的球形泡沫持续下落后反弹(图 3h)。之后在落点外其他位置也发生了几次类似的短促燃烧, 产生周围绿色中间明亮的火焰(图 3i), 同时, 白色的球形泡沫在下落后也发生反弹。这种短促燃烧可能与碰撞时的飞溅现象有关, 当少量离子液体飞溅到其他位置时, 迅速与周围的氧化剂混合, 发生化学反应后产生火焰。然而, 受莱顿弗罗斯特效应的影响, 液面上产生蒸汽层, 使得较大的离子液滴与RFNA很难混合, 只能利用海绵状结构的泡沫壳体吸收氧化剂蒸汽与内部剩余燃料持续反应[15], 经过较长时间的中间气相产物积累, 并且局部温度不断上升, 达到一定着火条件时, 白色球形泡沫变黑, 1167 ms(图 3j)时出现火焰核心, 靠近液面的火焰呈明亮的颜色, 上部为红色, 火焰持续大约95 ms。
I.L.8与两种发烟硝酸反应现象不同, 主要是由于两种发烟硝酸的成分差异(HNO3和NO2的含量不同)造成的。I.L.8与WFNA反应时, 碰撞后初期的反应明显更为剧烈, 在很短时间内有大量的二次液滴飞溅, 这也加速了后续的气相反应, 整个反应过程中只有少量的黑色烟气生成。Chambreau等[16]的研究表明, 离子液体与发烟硝酸反应的第一步为质子化反应, 从而破坏离子液体本身的结构, 使得后续的氧化反应可以更快速进行。因此HNO3含量更多的WFNA作为氧化剂与离子液体反应时的液相反应会更加剧烈, 使得自着火反应的点火延迟更短。而I.L.8与RFNA的反应初期只有少量的相对较大的二次液滴飞溅, 由于没有快速的初期反应来消耗离子液滴, 剩余的离子液滴受到莱顿弗罗斯特蒸汽层的影响与氧化剂很难混合充分, 只能在液滴表面和内部进行反应, 此时当地温度受到环境影响较大, 有大量的热量散失到空气中[15]。而几次短促的燃烧过后又产生黑色烟气, 同时提高氧化剂温度, 加速RFNA汽化, 继续抑制离子液滴与RFNA混合, 因此在很长的一段时间后剩余的离子液滴发生自着火。这与RFNA中HNO3含量较少但NO2含量较多有关, 较少的HNO3使得反应初期的液相反应较为缓慢, 而NO2和气象产物等一起组成了莱顿弗罗斯特蒸汽层, 阻碍了反应后的离子液滴与氧化剂进一步反应, 大量的热量散失, 大大增加了点火延迟。
3.2 阳离子结构对自着火的影响 3.2.1 阳离子中杂环的影响以阳离子杂环上具有相同的丁基侧链的I.L.2、I.L.5和I.L.7为例, 通过对比这三种离子液体与WFNA反应的过程, 探究阳离子中杂环是否影响离子液体/WFNA自着火反应的现象及时间参数。
图 4为I.L.2、I.L.5和I.L.7与WFNA反应的过程。由图 4可见, 这三种离子液体与WFNA均能发生自着火反应, 且I.L.2与WFNA反应的过程与I.L.8相似:在离子液滴与氧化剂液池接触0.72 ms后, 液滴发生微爆, 大量的二次小液滴高速向四周飞溅, 3.29 ms时出现火焰核心, 呈明亮的绿色和白色, 火焰持续大约100 ms后结束。而I.L.5和I.L.7与WFNA反应出现了两次着火的现象, 即液滴碰池经过诱导期后先形成一个小火球, 随后湮灭, 但经一段时间后又出现着火并燃烧的现象。进一步对这种出现两次着火的情况进行了仔细核查, 发现这种现象具有高度的重复性。以I.L.5与WFNA反应过程为例:离子液滴在0.86 ms时出现微爆, 2.86 ms左右第一次出现火焰核心, 而这次火焰持续时间和蔓延距离较短, 在17.87 ms时, 剩余的离子液体坐落在液面上, 这与I.L.8与RFNA反应的多次燃烧情况类似, 离子液滴与氧化剂的反应被莱顿弗罗斯特蒸汽层所抑制, 反应在泡沫状液滴的内部及表面上进行, 经过较长时间, 温度及气相产物浓度的积累达到合适条件, 在111 ms左右再次出现火焰核心, 火焰面积发展到最大时靠近液面的火焰呈明亮的颜色, 上部为红色, 火焰持续大约150 ms。

|
图 4 具有相同丁基侧链的I.L.2、I.L.5和I.L.7与WFNA反应的滴落实验现象 Fig.4 Droplet test phenomena of I.L.2, I.L.5 and I.L.7 which have the same butyl side chain reacted with WFNA |
由图 4可知, I.L.5和I.L.7与WFNA反应初期的微爆现象相较于I.L.2与WFNA反应的微爆现象更弱, 二次液滴飞溅的速度更慢, 飞溅面积更小, 使得进一步反应产生的气相产物更少, 导致初次的火焰只能消耗很少的离子液滴燃料, 而反应生成的气体及气化的WFNA形成的莱顿弗罗斯特蒸汽层抑制了剩余的离子液滴与WFNA的反应, 使得二次着火延迟时间较长。
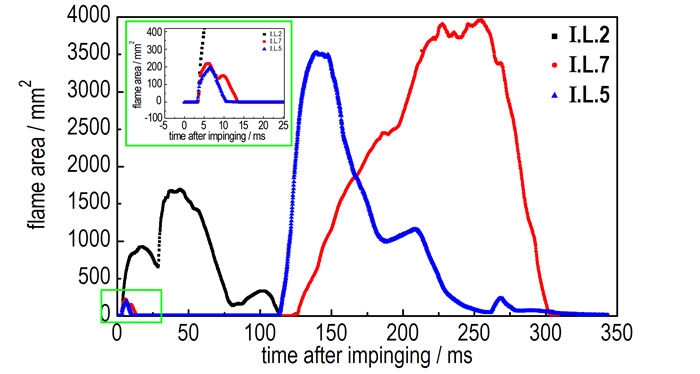
图 5为I.L.2、I.L.5和I.L.7与WFNA反应过程中生成的火焰面积随时间的变化关系, 从图 5可以看出I.L.2与WFNA的自着火反应生成的火焰面积较小, 且持续时间也较短。而I.L.5和I.L.7与WFNA自点火的火焰面积随时间变化曲线出现了前期一个较小峰值和后期一个较大峰值的情况, 这种现象的原因正是前文讨论的二次着火现象。第二次燃烧火焰面积较大, 持续时间也较长。火焰面积从一定程度上可以反映燃烧的放热量, 火焰面积越大且持续时间越长, 反应放出的热量越多, 燃烧特性更良好, 但实际推进剂应用中需要避免二次燃烧。
|
图 5 具有相同丁基侧链的I.L.2、I.L.5和I.L.7与WFNA反应的火焰面积随时间的变化 Fig.5 Change in flame area of I.L.2, I.L.5 and I.L.7 which have the same butyl side chain reacted vs WFNA vs. time |
选取阳离子中具有相同的吡啶杂环, 但是侧链不同的I.L.4和I.L.5、I.L.6三种离子液体与WFNA反应的实验现象, 分析它们与WFNA反应的过程以判断侧链对自着火的可能影响。
图 6为I.L.4、I.L.5和I.L.6与WFNA反应的过程。首先, 这三种离子液体与WFNA均能发生自着火反应, 且I.L.2和I.L.6与WFNA反应的过程与I.L.8一致, 以I.L.6与WFNA反应过程为例:离子液滴在0.43 ms时出现微爆, 大量的二次液滴高速飞溅, 1.86 ms左右出现火焰核心, 白色的球形泡沫状液滴不断被消耗, 火焰最初呈现出四周绿色中间明亮的白色, 随着火焰不断发展, 靠近液面的火焰呈明亮的颜色, 火焰上部为红色, 有絮状固体产物生成, 火焰持续大约170 ms。

|
图 6 具有相同吡啶杂环的I.L.4和I.L.5、I.L.6与WFNA反应的滴落实验现象 Fig.6 Droplet test phenomena of I.L.4, I.L.5 and I.L.6 which have the same pyridine heterocyclic core reacted with WFNA |
由图 6可知, 阳离子中分别含有乙基和丙烯基的I.L.4和I.L.6与WFNA反应初期的微爆延迟时间较短, 程度更加剧烈, 飞溅面积更大; 而含有丁基侧链的I.L.5与WFNA反应的微爆延迟时间相对较长, 并且出现了二次着火的现象。
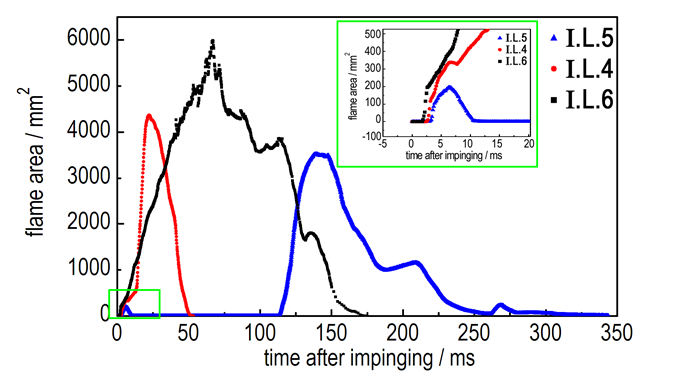
图 7为I.L.4、I.L.5和I.L.6与WFNA反应过程中生成的火焰面积随时间的变化关系图, 从图 7可以看出I.L.4与WFNA的自着火反应生成的火焰面积较小, 且持续时间也较短。而I.L.6与WFNA反应中的火焰面积最大, 持续时间也最长, 但是燃烧后有固体产物残留, 不利于应用到实际推进剂中。
|
图 7 具有相同吡啶杂环的I.L.4和I.L.5、I.L.6与WFNA反应的火焰面积随时间的变化 Fig.7 Change in flame area of I.L.4, I.L.5 and I.L.6 which have the same pyridine heterocyclic core reacted with RFNA vs. time |
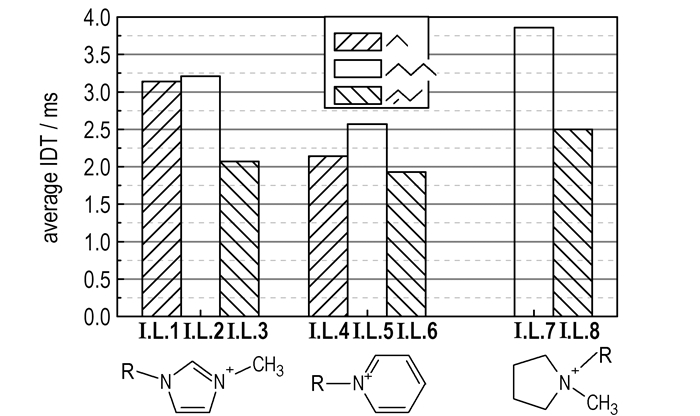
文献[9]表明, 阴离子是影响离子液体和氧化剂反应后的自着火过程和着火延迟时间的最重要因素, 同时, 也有学者研究了阳离子对于二氰胺等离子液体的自着火参数影响。图 8为实验用8种新型[BH3(CN)BH2(CN)]-基离子液体与WFNA反应的IDT随阳离子结构的变化关系图。由图 8可知, 首先, 对于具有相同杂环核心的[BH3(CN)BH2(CN)]-基的离子液体, 侧链上具有烯丙基的离子液体表现出最低的IDT, 随后是侧链上具有乙基的离子液体, 侧链上带有丁基的离子液体与WFNA反应的IDT最长。对于含有相同侧链的离子液体, 具有吡啶杂环的离子液体表现出最低的IDT, 随后是具有咪唑杂环的离子液体和具有吡咯烷的离子液体。
|
图 8 实验中8种新型[BH3(CN)BH2(CN)]-基离子液体与WFNA反应的点火延迟随阳离子结构的变化 Fig.8 Change in ignition delay time(IDT) of 8 newly synthesized [BH3(CN)BH2(CN)]- based I.L.s reacted vs. WFNA with cation structures |
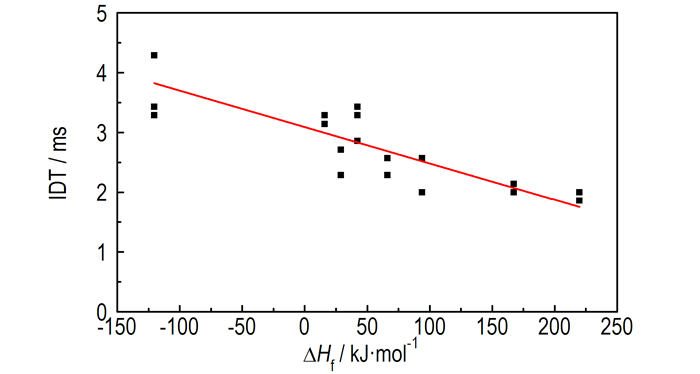
图 9为实验用8种新型[BH3(CN)BH2(CN)]-基离子液体与WFNA反应的IDT随生成焓的变化关系图。由图 9可以看出, 生成焓越高的离子液体与WFNA反应时表现出越短的IDT。因此, 离子液体的阳离子可能通过调节离子液体的生成焓, 进一步影响与氧化剂反应的IDT。
|
图 9 实验中8种新型[BH3(CN)BH2(CN)]-基离子液体与WFNA反应的点火延迟随生成焓的变化 Fig.9 Change in IDT of 8 newly synthesized [BH3(CN)BH2(CN)]- based I.L.s reacted vs. WFNA with heat of formation |
(1) 8种离子液体与白烟硝酸和红烟硝酸均获得稳定的自着火反应, 并且观察到两种不同的火焰发展过程。其中, I.L.8与白烟硝酸接触后发生微爆, 大量的二次液滴高速向四周飞溅, 加速了液相反应和气相产物生成, 导致在2.7 ms时出现气相火焰核心, 随后火焰迅速传播; 而I.L.8与红烟硝酸接触后发生二次液滴飞溅, 由于莱顿弗罗斯特效应的影响, 反应后的泡沫状液滴反弹并在99.6 ms时首次出现火焰核心, 但其传播仅持续4.7 ms, 几次短促燃烧后, 1167 ms时出现持续时间较长的火焰传播;
(2) 对于杂环核心相同的离子液体, 侧链上含有烯丙基的离子液体点火延迟时间最短(1.9~2.5 ms), 其次是含有乙基的离子液体(2.2~3.2 ms), 而含有丁基的离子液体与白烟硝酸反应的点火延迟时间最长(2.6~3.8 ms); 对于侧链相同的离子液体, 含有吡啶杂环的离子液体点火延迟时间最短(1.9~2.6 ms), 其次是含有咪唑杂环的离子液体(2.2~3.2 ms), 而含有四氢吡咯的离子液体与白烟硝酸反应的点火延迟时间最长(2.5~3.8 ms);
(3) 生成焓越高的离子液体, 点火延迟时间越短, 近似呈线性变化。
| [1] |
张光全. 离子液体在含能材料领域的应用进展[J].
含能材料, 2012, 20(2): 240-247. ZHANG Guang-quan. Application progress of ionic liquid in energetic marerials[J]. Chinese Journal of Energetic Materals(Hanneng Cailiao), 2012, 20(2): 240-247. |
| [2] |
Kang H, Won J, Baek S W, et al. Autoignition and combustion characteristics of sodium borohydride-based non-toxic hypergolic fuel droplet at elevated temperatures[J].
Combust Flame, 2017, 181: 149-156. DOI:10.1016/j.combustflame.2017.03.021 |
| [3] |
McLean C H, Hale M J, Deininger W D, et al. Green propellant infusion mission program overview[C]//49th AIAA/ASME/SAE/ASEE Joint Propulsion Conference. San Jose, CA. 2013.
|
| [4] |
Pasini A, Torre L, Pace G, et al. Pulsed chemical rocket with green high performance propellants [C]//49th AIAA/ASME/SAE/ASEE Joint Propulsion Conference. San Jose, CA. 2013.
|
| [5] |
Hongjae K, Sejin K. Development of 500 N scale green hypergolic bipropellant thruster using hydrogen peroxide as an oxidizer[C]//51st AIAA/SAE/ASEE Joint Propulsion Conference. Orlando, FL, USA. 2015.
|
| [6] |
Ramachandran P V, Kulkarni A S, Pfeil M A, et al. Amine-boranes: green hypergolic fuels with consistently low ignition delays[J].
Chem-Eur J, 2014, 20(51): 16869-16872. DOI:10.1002/chem.201405224 |
| [7] |
Melof B, Grubelich M. Investigation of hypergolic fuels with hydrogen peroxide[C]//37th AIAA/ASME/SAE/ASEE Joint Propulsion Conference. Salt Lake City, UT, U[Sun, 2017 #136]SA. 2001.
|
| [8] |
田均均, 张庆华. 含能离子液体——新型离子炸药和绿色推进剂燃料[J].
含能材料, 2014, 22(5): 580-581. TIAN Jun-jun, ZHANG Qing-hua. Energetic ionic liquids- new explosives and green propellant fuels[J]. Chinese Journal of Energetic Materals(Hanneng Cailiao), 2014, 22(5): 580-581. |
| [9] |
Zhang Q, Shreeve J n M. Energetic ionic liquids as explosives and propellant fuels: a new journey of ionic liquid chemistry[J].
Chem Rev, 2014, 114(20): 10527-10574. DOI:10.1021/cr500364t |
| [10] |
Zhang W, Qi X, Huang S, et al. Super-base-derived hypergolic ionic fuels with remarkably improved thermal stability[J].
J Mater Chem A, 2015, 3(41): 20664-20672. DOI:10.1039/C5TA05559H |
| [11] |
Liu T, Qi X, Huang S, et al. Exploiting hydrophobic borohydride-rich ionic liquids as faster-igniting rocket fuels[J].
Chem Commun, 2016, 52(10): 2031-2034. DOI:10.1039/C5CC09737A |
| [12] |
Schneider S, Hawkins T, Rosander M, et al. Ionic liquids as hypergolic fuels[J].
Energy Fuels, 2008, 22(4): 2871-2872. DOI:10.1021/ef800286b |
| [13] |
Sun C, Tang S, Zhang X. Role of cation structures for energetic performance of hypergolic ionic liquids[J].
Energy Fuels, 2017, 31(9): 10055-10059. DOI:10.1021/acs.energyfuels.7b01259 |
| [14] |
Manzello S L, Yang J C. An experimental study of a water droplet impinging on a liquid surface[J].
Exp Fluids, 2002, 32(5): 580-589. DOI:10.1007/s00348-001-0401-8 |
| [15] |
Li J, Fan W, Weng X, et al. Experimental observation of hypergolic ignition of superbase-derived ionic liquids[J].
J Propul Power, 2018, 34(1): 125-132. DOI:10.2514/1.B36441 |
| [16] |
Chambreau S D, Koh C J, Popolanvaida D M, et al. Flow-tube investigations of hypergolic reactions of a dicyanamide ionic liquid via tunable vacuum ultraviolet aerosol mass spectrometry[J].
J Phys Chem A, 2016, 120(41): 8011-8023. DOI:10.1021/acs.jpca.6b06289 |

To determine whether the novel I.L.s can self-ignite with WFNA and RFNA, explain the phenomenon of the hypergolic ignition and compare the difference between the reactions of I.L.s-WFNA and I.L.s-RFNA, explore the factors affecting the ignition delay time of the hypergolic process, the reactions of 8 ionic liquids with WFNA and RFNA respectively were tested using the long focus microscope-high speed photography techniques.





