近年来, 含两个及两个硝基以上吡唑类含能化合物由于其高能量, 爆轰性能优异及低敏感度的特性得到了广泛关注[1]。1-氢-3, 5-二硝基吡唑, 熔点173 ℃, 分解温度317 ℃, 密度1.80 g·cm-3, 爆热800.45 kJ·mol-1[2], 具有较高的热稳定性和化学稳定性, 是典型的二硝基吡唑类化合物的含能结构单元[3]。除硝基的引入外, 氨基的引入也可以提高吡唑类含能化合物的性能。引入的氨基, 很可能与硝基形成分子内和分子间的氢键, 进一步提高化合物的密度, 降低其感度[4]。其中N—NH2的引入可以提高化合物的生成热, 降低其感度; C—NH2的引入可以提高其密度、爆速、爆压等[5]。美国Livemore国家实验室于2001年首次合成了4-氨基-3, 5-二硝基吡唑(LLM-116)。LLM-116感度较低, 能量是1, 3, 5-三氨基-2, 4, 6-三硝基苯(TATB)的1.38倍, 是一种性能优异的新型含能材料, 在不敏感弹药中具有潜在的应用前景[6]。
1971年, 4-溴-3, 5-二硝基-1-甲基-吡唑首次被合成[7], 成为合成其他3, 5-二硝基吡唑化合物的重要中间体, 但是该反应步骤繁琐, 收率仅有26%。本实验以吡唑为原料通过卤化、硝化反应得到合成3, 5-二硝基吡唑类化合物的重要中间体4-氯-3, 5-二硝基吡唑(CDNP), 获得较高收率。再以CDNP为前体经过胺化反应合成1, 4-二氨基-3, 5-二硝基吡唑(DADNP)。DADNP在LLM-116结构中引入N—NH2, 消除了LLM-116的酸性, 也提高了LLM-116的热安定性。
2 实验部分 2.1 试剂与仪器试剂:对甲基苯磺酰羟胺(THA), 2, 4, 6-三甲基苯磺酰羟胺(MSH), 自制[8-9]; 吡唑、N-氯代丁二酰亚胺、羟胺-O-磺酸, 均为分析纯, 安耐吉化学; 氢氧化钠、氨水、二氯甲烷、乙酸乙酯等试剂均为分析纯, 南京化学试剂有限公司。
仪器:Bruker Avance-Ⅲ 500 MHz数字化核磁共振仪(瑞士), Thermo Fisher Scientific Trace 1300气质联用仪(美国), Vario EL-Ⅲ元素分析仪(德国), Agilent 1200高效液相色谱仪(美国), TA Q-200差式扫描量热仪(美国)。
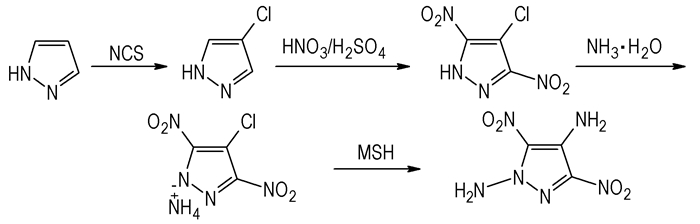
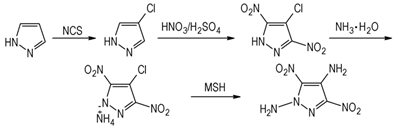
2.2 合成路线合成路线见Scheme 1。
|
Scheme 1 Synthesis route of 1, 4-diamino-3, 5-dinitropyrazole |
将3.40 g(50 mmol)吡唑加入盛有100 mL四氯化碳的250 mL单口烧瓶中, 在室温搅拌下, 加入6.80 g(50 mmol) N-氯代丁二酰亚胺(NCS), 反应12 h, 析出白色固体, 过滤, 滤液用水洗涤(2×20 mL), 无水硫酸钠干燥, 减压蒸馏得4.21 g白色固体产物, 收率82.5%, 纯度99.5%(HPLC)。1H NMR(DMSO-d6, 500 MHz)δ:13.07(Br, NH), 7.76(s, CH)。13C NMR(DMSO-d6, 125 MHz)δ:132.33, 108.62。
2.3.2 4-氯-3, 5-二硝基吡唑(CDNP)的合成冰浴搅拌下, 将4.10 g(40 mmol) 4-氯吡唑加入盛有15 mL 20%发烟硫酸的100 mL三口烧瓶中, 缓慢滴加由20 mL浓硝酸和25 mL浓硫酸组成的混酸, 控制滴加温度不超过45 ℃。滴加完毕, 反应体系升温至110~115 ℃, 反应5 h, 冷却, 倒入100 mL冰水中, NaOH水溶液调节pH=7, 乙酸乙酯萃取, 无水硫酸钠干燥, 减压蒸馏得5.53 g白色固体, 收率72.0%, 纯度99.0%(HPLC)。1H NMR(DMSO-d6, 500 MHz)δ:8.56(Br, NH)。13 C NMR(DMSO-d6, 125 MHz)δ:151.49, 100.61。
2.3.3 4-氨基-3, 5-二硝基吡唑铵盐一水合物(ADNP-NH4+)的合成将0.96 g(5 mmol) 4-氯-3, 5-二硝基吡唑加入盛有15 L浓氨水的35 mL耐压管中, 加热至130 ℃, 反应12 h, 冷却, 倒入冰水中, 析出橙色晶体, 抽滤, 冰水洗涤, 真空干燥得0.74 g橙色针状固体, 收率77.8%, 纯度99.9%(HPLC)。1H NMR(DMSO-d6, 500 MHz)δ:7.08(s, NH4+), 6.56(s, NH2)。13C NMR(DMSO-d6, 125 MHz)δ:144.15, 132.49。
2.3.4 1, 4-二氨基-3, 5-二硝基吡唑(DADNP)的合成室温搅拌下, 将1.90 g(10 mmol)4-氨基-3, 5-二硝基吡唑铵盐加入盛有125 mL乙腈的250 mL单口烧瓶中, 逐滴加入预先配制好的MSH(3.23 g, 15 mmol)的乙腈溶液, 室温反应12 h, 减压蒸馏, 得粗产物, 用乙醇重结晶, 得1.04 g橙色粉末, 收率58.0%, 纯度99.0%(HPLC)。m.p.192~194 ℃。1H NMR(DMSO-d6, 500 MHz)δ:7.91(Br, N—NH2), 7.25(s, C—NH2)。13C NMR(DMSO-d6, 125 MHz)δ:133.48, 129.69, 127.46。IR(KBr, ν/cm-1):3469, 3343, 3249, 1621(—NH2), 1557, 1500, 1371, 1308(—NO2), 1462, 855, 773(Pyrazole)。MS(EI, m/z):188(M+)。元素分析(%), C3H4N6O4:实测值(计算值) C 19.12(19.16), H 2.09(2.14), N 44.62(44.68)。
3 结果与讨论 3.1 4-氯-3, 5-二硝基吡唑(CDNP)的合成工艺优化对合成重要前体4-氯-3, 5-二硝基吡唑(CDNP)的硝化反应进行了研究。对影响硝化反应的三个主要因素因:反应时间、发烟硫酸用量、反应温度的条件进行了优化。
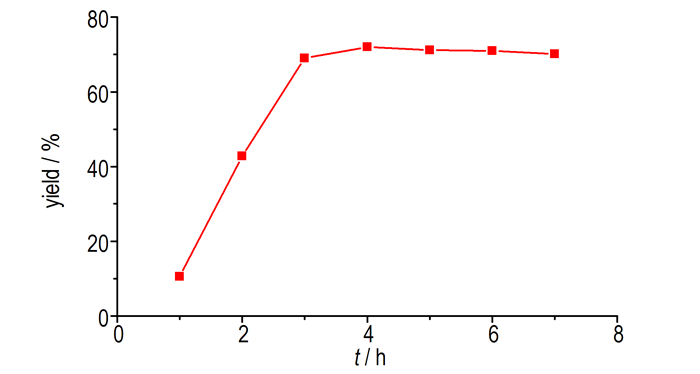
3.1.1 反应时间对CDNP收率的影响反应时间是影响硝化反应的一个重要因素, 影响着反应收率及生产周期的长短。在反应温度为110~115 ℃, V(硫酸):V(硝酸)=2:1条件下, 考察了反应时间对硝化反应收率的影响。结果如图 1所示。
|
图 1 反应时间对CDNP收率的影响 Fig.1 Effect of reaction time on the yield of CDNP |
图 1表明, 随着反应时间延长, CDNP的收率表现出先增加后稳定的趋势, 4-氯吡唑的硝化过程分两步, 反应时间过短, 导致4-氯吡唑不能完全转化且生成一硝基取代副产物。当反应时间为4 h时, 收率达到72.0%, 再延长反应时间对收率影响不大。综合产品收率和合成成本因素, 较佳反应时间为4 h。
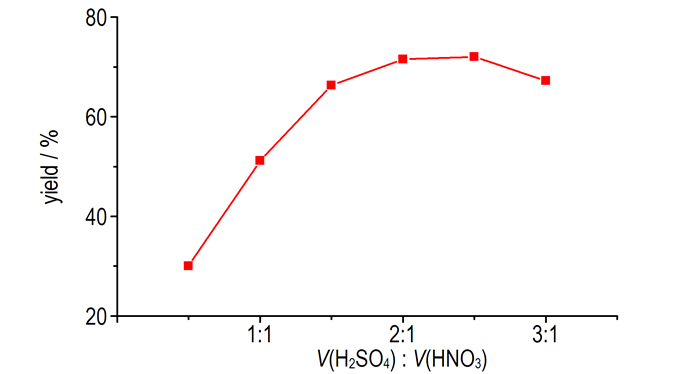
3.1.2 发烟硫酸用量对CDNP收率的影响发烟硫酸不仅是硝化反应中硝化体系的组成部分, 也作为反应体系的溶剂, 发挥着重要作用。合适用量的发烟硫酸不仅是硝化反应进行的保障, 同时可减少后期废水处理量。在反应温度为110~115 ℃, 反应时间为4 h的条件下, 考察不同发烟硫酸用量对CDNP合成收率的影响, 结果如图 2所示。
|
图 2 发烟硫酸用量对CDNP收率的影响 Fig.2 Effect of oleum amount on the yield of CDNP |
图 2表明, 随着发烟硫酸用量的增大, CDNP合成收率先增大后减小, 在V(硫酸):V(硝酸)=2:1~2.5:1时收率较高, 达到70%。发烟硫酸用量过少, 不利于NO2+的产生, 收率较低。当V(硫酸):V(硝酸)>2.5:1, 发烟硫酸量的增加可能导致体系中NO2+浓度减小, 硝化收率降低。综合以上分析, 选取合适的发烟硫酸体积与发烟硝酸的体积比为2:1。
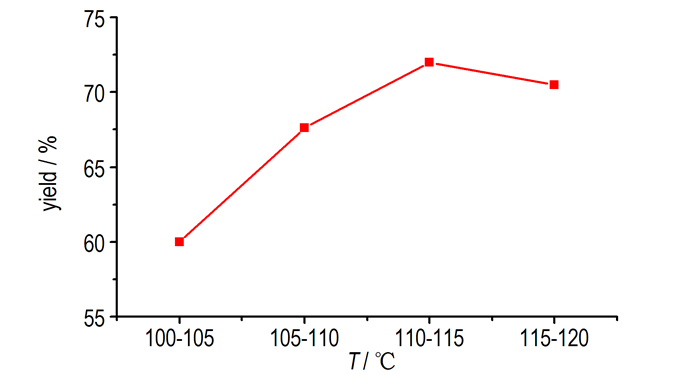
3.1.3 反应温度对CDNP收率的影响在反应时间为4 h, V(硫酸):V(硝酸)=2:1条件下, 考察了反应温度对硝化反应收率的影响, 结果如图 3所示。
|
图 3 反应温度对CDNP收率的影响 Fig.3 Effect of reaction time on the yield of CDNP |
图 3表明, 随着反应温度的增加, CDNP的收率先增加后有所减少。当反应温度为110~115 ℃时, 收率达到最高。反应温度的升高可以提高反应速率, 缩短反应达到平衡的时间, 提高原料的转化率, 但同时会导致发烟硝酸分解加剧, 实验选择110~115 ℃为最佳的反应温度。
3.2 胺化反应影响因素 3.2.1 胺化试剂对DADNP收率的影响目前常见的N-胺化试剂有羟胺-O-磺酸(HOSA)、2, 4, 6-三甲基苯磺酰羟胺(MSH)、对甲基苯磺酰羟胺(THA)等。在n(ADNP-NH4+):n(胺化试剂)=1:1, 室温, 反应时间为12 h条件下, 考察了不同胺化试剂对DADNP收率的影响, 结果见表 1。
| 表 1 胺化试剂对DADNP收率的影响 Tab.1 Effect of N-amination reagents on the yield of DADNP |
从表 1可以看出, HOSA作为胺化试剂该反应不能发生, MSH作为胺化试剂的收率稍高于THA。这是因为HOSA反应活性较低, 常用于富电子氮杂环化合物的胺化[10]。MSH、THA反应活性较高, 多用于含缺电子基团氮杂环化合物的氮胺化[11], THA在干燥状态下很不稳定, 容易分解, MSH的稳定性较好, 所以较佳的胺化试剂为2, 4, 6-三甲基苯磺酰羟胺(MSH)。
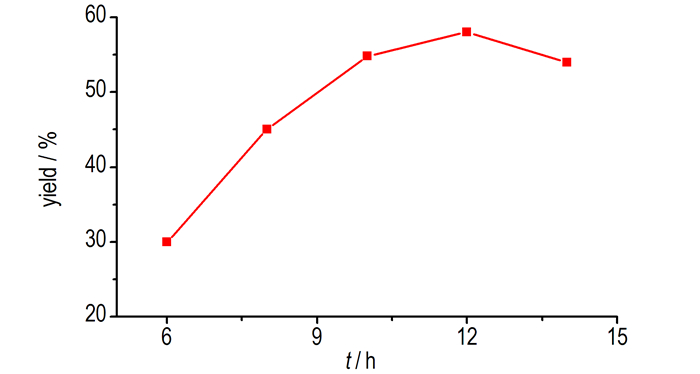
3.2.1 反应时间对DADNP收率的影响在胺化试剂为MSH, n(ADNP-NH4+):n(MSH)=1:1, 室温条件下, 考察了反应时间对DADNP收率的影响, 结果如图 4所示。
|
图 4 反应时间对DADNP收率的影响 Fig.4 Effect of reaction time on the yield of DADNP |
图 4表明, 当反应时间为12 h, 收率较高, 达到55.0%。随着反应时间延长, 收率无明显提高, 因此, 较适宜的反应时间为12 h。
3.2.2 物料比对DADNP收率的影响在胺化试剂为MSH, 室温条件下, 反应时间为12 h, 考察了MSH用量对DADNP收率的影响, 结果如图 5所示。

|
图 5 物料比对DADNP收率的影响 Fig.5 Effect of materials ratio on the yield of DADNP |
图 5表明, 当n(ADNP-NH4+):n(MSH)=1:1.5时, 收率最高, 达到58.0%。由于MSH在室温条件下会有少量分解, 且随着反应时间延长, 分解量会进一步增加。因此, 反应体系需要加入过量的MSH, 故n(ADNP-NH4+):n(MSH)=1:1.5最优。
3.3 DADNP的热分性能分析在N2流速为30 mL·min-1, 升温速率为10.0 ℃·min-1, 温度为50~400 ℃条件下获得了DADNP的差示扫描量热(DSC)曲线, 如图 6所示。

|
图 6 DADNP的DSC曲线 Fig.6 DSC curve of DADNP |
从图 6可以看出, 曲线在182 ~197 ℃有一个吸热峰, 峰温为192 ℃, 与样品所测的熔点192 ~194 ℃一致, 为DADNP的熔点。从225 ℃开始放热, 在244 ~251 ℃形成一个较大的放热峰, 峰顶温度为247 ℃。LLM-116的熔点在175 ~176 ℃, 峰顶温度为183 ℃[12]。DADNPA与LLM-116相比, 峰顶温度提高了64 ℃, 表明其热稳定性优于LLM-116。
4 结论(1) 以4-氯-3, 5-二硝基吡唑(CDNP)为前体, 用2, 4, 6-三甲基苯磺酰羟胺(MSH)为胺化试剂, 得到了目标产物1, 4-二氨基-3, 5-二硝基吡唑(DADNP), 收率58.0%。DADNP的较佳合成条件:室温, n(ADNP-NH4+):n(MSH)=1:1.5, 反应时间12 h。
(2) 采用DSC研究了DADNP的热分解性能, 其熔点为192 ℃, 分解峰温为247 ℃, 表明DADNP热安定性比较好。
| [1] |
Gao H, Shreeve J M. Azole-based energetic salts[J].
Chemical Reviews, 2011, 111: 7377-7436. DOI:10.1021/cr200039c |
| [2] |
Pagoria P F, Lee G S, Mitchell A R, et al. A review of energetic materials synthesis[J].
Thermochimica Acta, 2002, 384: 187-204. DOI:10.1016/S0040-6031(01)00805-X |
| [3] |
汪营磊, 张志忠, 王伯周, 等. 3, 5-二硝基吡唑合成研究[J].
含能材料, 2007, 15(6): 574-576. WANG Ying-lei, ZHANG Zhi-zhong, WANG Bo-zhou, et al. Synthesis of 3, 5-dinitropyrazole[J]. Chinese Journal of Energetic Materials(Hanneng Cailiao), 2007, 15(5): 574-576. |
| [4] |
蒋涛, 张晓玉, 景梅, 等. 1-氨基-3, 5-二硝基吡唑的合成、晶体结构及热性能[J].
含能材料, 2014, 2(5): 654-657. JIANG Tao, ZHANG Xiao-yu, JING Mei, et al. Synthesis, Crystal structure and thermal property of 1-amino-3, 5-dinitropyrazole[J]. Chinese Journal of Energetic Materials(Hanneng Cailiao), 2014, 2(5): 654-657. |
| [5] |
ZHAO Xiu-xiu, QI Cai, ZHANG lu-bo, et al. Amination of nitroazoles-a comparative study of structual and energetic properties[J].
Molecules, 2014, 19: 896-910. DOI:10.3390/molecules19010896 |
| [6] |
王伯周, 汪营磊, 张志忠, 等. 4 -氨基-3, 5 -二硝基吡唑﹙LLM-116﹚缩合物的合成与表征[J].
含能材料, 2009, 17(3): 293-295. WANG Bo-zhou, WANG Ying-lei, ZHANG Zhi-zhong, et al. Synthesis and characterization of 4-amino-3, 5-dinitropyrazole(LLM-116) condensation products[J]. Chinese Journal of Energetic Materials(Hanneng Cailiao), 2009, 17(3): 293-295. |
| [7] |
Coburn M D. 3, 5-Dinitropyrazoles[J].
Journal of Heterocyclic Chemistry, 1971, 8: 153-154. DOI:10.1002/(ISSN)1943-5193 |
| [8] |
Willardsen, J Adam, Lockman, et al. Preparation of urea compounds as Nampt inhibitors and their use in the treatment of cancer. USP 13708235[P], 2013.
|
| [9] |
李亚南, 李祥志, 刘宁, 等. N-胺化试剂MSH、PHA的合成、表征及热性能[J].
化学试剂, 2014, 36(9): 788-790. LI Ya-nan, LI Xiang-zhi, LIU Ning, et al. Synthesis and thermal property of N-amination reagents MSH and PHA[J]. Chemical Reagents, 2014, 36(9): 788-790. |
| [10] |
Thomas M K, Piercey D G, Stierstorfer J. Amination of energetic anions:high performing energetic materials[J].
Dalton Transactions, 2012, 41: 9451-9459. DOI:10.1039/c2dt30684k |
| [11] |
PING Yin, ZHANG Qing-hua, ZHANG Jia-heng, et al. N-trinitroetylamino functionalization of nitro midazoles:a new strategy for high performance energetic materials[J].
Journal of Materials Chemistry A, 2013(1): 7500-7510. |
| [12] |
Schmidt R D, Lee G S, Pagoria P F, et al. Synthesis of 4-amino-dinitro-1H-pyrazole using vicarious nucleophilic substitution of hydrogen[J].
Journal of Heterocyclic Chemistry, 2001, 38(5): 1227-1230. DOI:10.1002/jhet.v38:5 |
1, 4-Diamino-3, 5-dinitropyrazole was synthesized from pyrazole via halogenation, nitration and amination reaction. The thermal behavior was studied by DSC.




