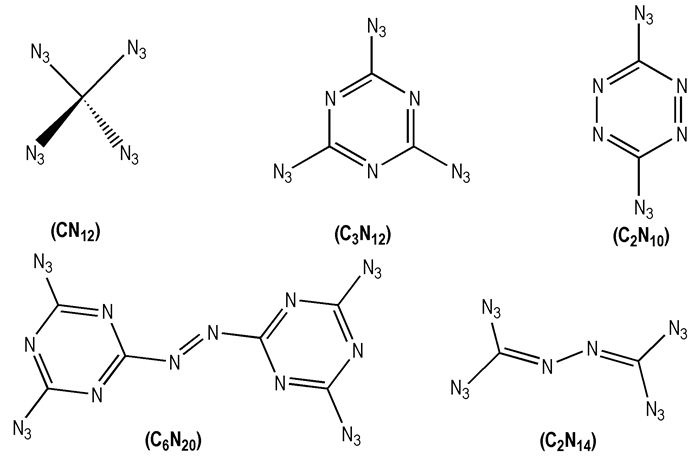
高氮化合物具有高密度[1-2]、高生成焓[3-5]、热稳定性好[6-8]等一系列优良的性质, 受到人们的广泛关注, 只含碳、氮两种元素的多叠氮类碳氮二元化合物更是研究的重点。例如, 四叠氮甲烷(CN12)[9]、2, 4, 6-三叠氮-1, 3, 5-三嗪(C3N12)[10]、3, 6-二叠氮-1, 2, 4, 5-四嗪(C2N10)[11-12]、4, 4′, 6, 6′-四叠氮基偶氮-1, 3, 5-三嗪(C6N20)[13-15]和四叠氮异氰(C2N14)[16]等, 分子结构如Scheme 1所示。
|
Scheme 1 |
其中, 四叠氮异氰(C2N14)自1961年成功合成以来备受研究者的关注。Banert等[17]通过实验发现, 四叠氮异氰的稳定性较差, 在低温下会经重排环化反应快速转化为它的同分异构体1-二叠氮甲基亚氨基-5-叠氮四唑(DACAT)。2011年, Klapötke等[18]首次利用三氨基胍盐酸盐为原料, 经重氮化取代反应、环化反应合成了DACAT, 并对其反应机理进行了推测。目前, 国内尚未见DACAT的研究报道。因此, 本研究根据文献报道的方法合成了DACAT, 并采用密度泛函理论(DFT)的B3LYP法[19]对其进行结构优化, 得到其稳定的几何构型和振动频率。然后应用Monte-Carlo方法[20]基于0.001 e·Bohr-3等电子密度面所包围的体积求得DACAT的理论密度; 采用原子化方案[21-24], 利用完全基组方法(CBS-4M)[25]计算了分子的气相生成焓, 对DACAT的静电势参数进行统计计算, 采用Politzer等人[26]提出的公式计算了分子的升华焓, 并获得DACAT的固相生成焓; 运用Kamlet-Jacobs[27]公式计算了DACAT的爆速和爆压, 并与TNT、RDX和HMX的性能进行了比较, 为DACAT在含能材料中的应用研究提供理论基础。
2 实验部分 2.1 材料及仪器材料:三氨基胍盐酸盐, 分析纯, 成都市科龙化工试剂厂; 亚硝酸钠, 分析纯, 成都市科龙化工试剂厂。
仪器:Nicolet傅里叶变换红外光谱仪, 美国Thermo Electron公司; Bruker核磁共振仪(TMS内标), 德国Bruker公司。
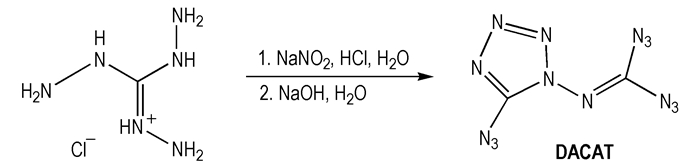
2.2 合成路线以三氨基胍盐酸盐为原料, 经重氮化取代反应、环化反应合成目标化合物DACAT, 合成路线见Scheme 2。
|
Scheme 2 |
将0.564 g(4 mmol)三氨基胍盐酸盐溶于60 mL蒸馏水, 加入2 mL 2 mol·L-1盐酸溶液, 然后将反应体系冷却至0 ℃, 滴加溶有0.556 g(8 mmol)亚硝酸钠的水溶液60 mL, 整个滴加过程持续30 min。滴毕, 将反应体系缓慢升至室温(20 ℃)并继续反应30 min。然后缓慢滴加0.1 mol·L-1的氢氧化钠溶液直至调节pH为8.0。滴加完成后, 用200 mL乙醚萃取反应物两次, 静置分层后分出有机相, 然后减压蒸除乙醚得无色透明液体。以氯仿为流动相, 将所得液体产物用柱色谱进行分离得无色晶体状DACAT 0.11 g(0.5 mmol), 产率12.6%。m.p.:78 ℃; IR(KBr, ν/cm-1):2156(—N3), 1726, 1578(C=N), 1529(C—N), 1459(N—N), 903(tetrazole ring); 13C NMR(CDCl3, 500 MHz, -10 ℃) δ:157.901(tetrazole ring), 148.276(N3—C—N3); 14N NMR(CDCl3, -10 ℃)δ:-145(tetrazole), -147(—N3), -148(—N3), -149(—N3)。
3 结果与讨论 3.1 体系酸碱性对收率的影响通过对反应条件的优化, 发现体系酸碱性是影响DACAT产物收率最关键的因素。故详细考察了体系酸碱性(pH值)对反应收率的影响, 结果见表 1。
| 表 1 pH值对DACAT收率的影响 Tab.1 Effect of pH on yield of DACAT |
由表 1可见, 当反应体系呈中性和酸性时, 无法得到目标化合物; 而只有当反应体系为碱性时, 二聚化反应和环化反应方能发生。由此可见, 碱性环境对该反应体系至关重要, 其原因在于如果反应体系处于酸性环境中, 体系残留或过量的亚硝酸钠产生的亚硝酸能够引起叠氮基的分解, 从而生成氨化的副产物[8]。表 1结果表明, pH值为8最优。
3.2 投料比对收率的影响固定总反应时间为60 min, 重氮化反应温度(Td)为0 ℃, 环化反应温度(Tc)为20 ℃, 反应体系pH=8.0, 考察了投料比[n(三氨基胍盐酸盐):n(亚硝酸钠)]对反应收率的影响, 结果见表 2。由表 2可知, 随着n(三氨基胍盐酸盐):n(亚硝酸钠)由1.0:1.0改变至1.0:2.0时, 反应收率逐渐提高。这可能是由于亚硝酸钠用量的增加有利于促进重氮化反应的进行; 而当继续增加亚硝酸钠用量后, 反应收率反而出现大幅度下降。这是因为过量的亚硝酸钠产生的亚硝酸导致了叠氮基的分解而生成氨化副产物[18]。结果表明, n(三氨基胍盐酸盐):n(亚硝酸钠)=1.0:2.0最佳。
| 表 2 投料比对DACAT收率的影响 Tab.2 Effect of molar ratio on yield of DACAT |
当n(三氨基胍盐酸盐):n(亚硝酸钠)=1.0:2.0, 反应体系pH=8.0时, 分别探究了重氮化反应温度(Td)和环化反应温度(Tc)对反应收率的影响, 结果见表 3。
| 表 3 反应温度对DACAT收率的影响 Tab.3 Effect of reaction temperature on yield of DACAT |
由表 3可见, 重氮化反应温度和环化反应温度对反应的收率都会产生影响。随着重氮化反应温度和环化反应的分别升高, 反应收率出现先升高后下降的变化趋势。可见, 两步反应温度过高均不利于目标化合物的生成。综合考虑二者变化趋势, 确定最佳反应温度分别为Td=0 ℃, Tc=20 ℃。
3.4 反应时间对收率的影响固定其它反应条件不变, 分别研究了重氮化反应时间(td)和环化反应时间(tc)对收率的影响, 见表 4。
| 表 4 反应时间对DACAT收率的影响 Tab.4 Effect of reaction time on yield of DACAT |
由表 4可见, 重氮化反应时间对反应收率影响较大, 而环化反应时间对反应收率的影响不明显。综合考虑, 确定最佳反应时间为td和td均为30 min。
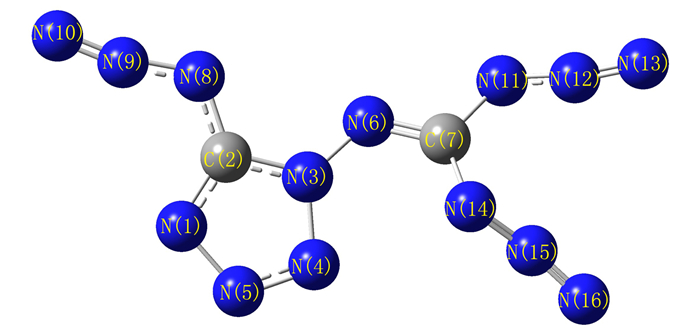
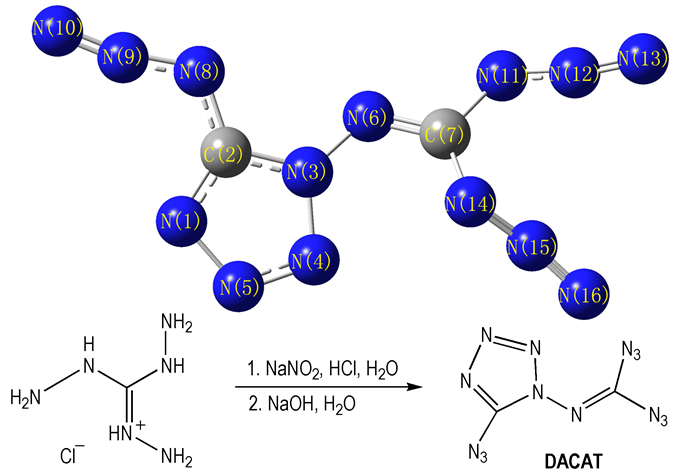
3.5 量子化学计算 3.5.1 几何优化在B3LYP/6-31G(d, p)基组水平下优化得到DACAT的几何结构, 优化后的几何构型及原子编号见图 1, 几何参数见表 5。经振动频率分析可知, 所得几何构型的振动分析无虚频, 表明其为势能面上的极小点, 为相对稳定构型。
|
图 1 DACAT的几何优化构型 Fig.1 The optimized structure of DACAT |
| 表 5 DACAT的部分几何参数 Tab.5 Selected geometric parameters of DACAT |
由优化得到的几何构型和表 5中二面角数据可知, DACAT结构中含有一个四唑环单元, 其中所有原子均具有较好的共面性, 环中所有键[N(1)—C(2), N(1)—N(5), N(2)—N(3), N(3)—N(4), N(4)—N(5)]的键长分别为1.3172, 1.3545, 1.3632, 1.3725Å和1.2856 Å, 接近C—N、C=N和N—N键的标准键长(1.4720, 1.2870Å和1.450Å)并趋于平均化, 表明四唑环中存在着较为明显的共轭作用, 有利于结构的稳定; 四唑环骨架原子的键角介于105°~112°, 偏离五元环上N或C取sp2杂化所要求的120°, 而接近于正五边形的内角108°, 说明四唑环内存在一定的张力。此外, 叠氮基中N(8)—N(9)、N(9)—N(10)、N(11)—N(12)、N(12)—N(13)、N(14)—N(15)、N(15)—N(16)的键长分别为1.2439, 1.1263, 1.2441, 1.1255, 1.2441Å和1.1229Å, 介于N=N和N≡N的标准键长(1.1000Å和1.2500Å)之间。
3.5.2 振动频率分析以B3LYP/6-31G(d, p)水平的优化构型为基础, 对DACAT进行了振动频率分析(校正因子为0.9614[2]), 结果表明DACAT不存在虚频, 为势能面上的极小点, 确定其为稳定结构构型。将理论红外光谱数据与实测值进行特征吸收峰比较, 见表 6。
| 表 6 DACAT的实测与理论特征红外光谱数据 Tab.6 Found and theoretical IR value of DACAT |
由表 6可知, DACAT的理论红外光谱与实测值较为吻合, 表明所选择的B3LYP/6-31G(d, p)基组水平对该化合物体系较为合适。
3.5.3 键级及稳定性分析在B3LYP/6-31G(d, p)基组水平下优化后的自然键轨道(NBO)分析所得C、N原子之间的键级见表 7。由表中数据可知, DACAT结构中, N(3)—N(4), N(3)—N(6), C(7)—N(11)和C(7)—N(14)四个键的键级基本相等且是整个分子中最小的, 说明这四个键均可作为该化合物的热解引发键。肖鹤鸣等[2]认为计算所得热解引发键的键离解能(BDE)可作为稳定性的定量标准。若BDE大于80 kJ·mol-1, 认为达到基本要求; 若BDE大于120 kJ·mol-1, 认为满足品优高能量密度材料的稳定性要求。通过计算得到的DACAT的热解引发键的BDE列于表 7。
| 表 7 DACAT的键级及热解引发键BDE Tab.7 Wiberg bond index of DACAT and its BDE |
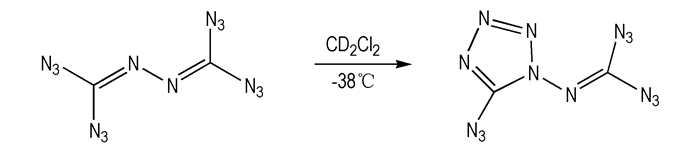
由表 7可知, DACAT中四个热解引发键N(3)—N(4), N(3)—N(6), C(7)—N(11)和C(7)—N(14)的BDE值均大于120 kJ·mol-1, 满足高能量密度材料的热力学稳定性要求。此外, Klaus Banert[17]等通过动态核磁共振方法研究了DACAT和四叠氮异氰的稳定性和相互转化关系。结果表明:四叠氮异氰的稳定性较差, 极易经环化反应转化为较稳定的DACAT, 且半衰期t1/2≤5 h, 其化学反应方程式如Scheme 3所示。
|
Scheme 3 |
本研究使用原子化能法, 利用完全基组方法(CBS-4M)对DACAT的气相生成焓和固相生成焓进行计算, 其中C、N原子在温度为298 K的生成焓取自文献值[28], 计算可得DACAT的气相生成焓ΔfH(g, M, 298 K)θ=1590.42 kJ·mol-1, 固相生成焓ΔfH(s, M, 298 K)θ=1435.44 kJ·mol-1。所得结果均进行振动分析确认无虚频, 表明其均为稳定构型的焓值。
3.5.5 爆轰性能爆速和爆压是含能材料最重要的爆轰性能。对于组成为CaHbNcOd的含能材料, Kamlet-Jacbos公式是估算其爆速和爆压较准确的经验公式:
| $ p = 1.558{\rho ^2}N{{\bar M}^{1/2}}{Q^{1/2}} $ | (1) |
| $ D = 1.01{(N{{\bar M}^{1/2}}{Q^{1/2}})^{1/2}}\left( {1 + 1.30\rho } \right) $ | (2) |
式中, p为爆压, GPa; D为爆速, km·s-1; Q为每克含能材料的最大爆热, J·g-1; N为每克含能材料的气体爆轰产物数量, mol·g-1; M为气体爆轰产物的平均摩尔质量, g·mol-1; ρ为含能材料的理论密度, g·cm-3。
首先, 采用Monte-Carlo法[20]计算出DACAT的摩尔体积。为了减小计算误差, 取100次计算值的平均值为目标化合物的摩尔体积Vm=129.3825 cm3·mol-1, 然后求得理论密度ρ =1.7628 g·cm-3。由此可求得目标化合物的爆速D=8725 m·s-1, 爆压p=34.52 GPa。将计算所得DACAT的爆轰性能参数与TNT、HMX和RDX的实验值[29-30]进行比较, 见表 8。
| 表 8 DACAT与几种炸药的爆轰性能参数 Tab.8 Detonation parameters of DACAT and other explosives |
由表 8可见, DACAT的密度高于常用炸药TNT和RDX, 爆速和爆压均优于TNT, 接近HMX和RDX的爆速。
4 结论(1) 以三氨基胍盐酸盐为原料, 经重氮化取代反应、环化反应合成目标化合物DACAT, 最佳反应条件为n(三氨基胍盐酸盐):n(亚硝酸钠)=1:2, 重氮化取代反应温度(Td)为0 ℃, 环化反应温度(Tc)为20 ℃, pH值为8.0, 重氮化反应时间(td)和环化反应时间(tc)均为30 min, 收率为12.6%。
(2) 采用密度泛函理论, 在B3LYP/6-31G(d, p)基组水平下优化得到DACAT的几何结构, 并在此基础上计算得到DACAT的红外光谱; 利用完全基组方法(CBS-4M)计算获得DACAT的气相生成焓和固相生成焓分别为1590.42 kJ·mol-1和1435.44 kJ·mol-1。
(3) 采用Monte-Carlo法计算获得DACAT的理论密度为1.7628 g·cm-3, 进而用Kamlet-Jacbos公式计算获得DACAT的爆速为8725 m·s-1, 爆压34.52 GPa。
| [1] |
Chavez D E, Hiskey M A, Gilardi R D. 3, 3'-Azobis(6-amino-1, 2, 4, 5-tetrazine):a novel high-nitrogen energetic material[J].
Angew Chem Int Ed, 2000, 39(10): 1791-1793. DOI:10.1002/(SICI)1521-3773(20000515)39:10<1791::AID-ANIE1791>3.0.CO;2-9 |
| [2] |
Kerth J, Lobbecke S. Synthesis and characterization of 3, 3'-azobis(6-amino-1, 2, 4, 5-tetrazine)DAAT-a new promising nitrogen-rich compound[J].
Propellants, Explos, Pyrotech, 2002, 27(3): 111-118. DOI:10.1002/1521-4087(200206)27:3<111::AID-PREP111>3.0.CO;2-O |
| [3] |
Huynh M H V, Hiskey M A, Hartline E L. Polyazido high-nitrogen compounds:hydrazo-and azo-1, 3, 5-triazine[J].
Angew Chem Int Ed, 2004, 43(37): 4924-4928. DOI:10.1002/(ISSN)1521-3773 |
| [4] |
Zhou G, Zhang J L, Wong N B, et al. Computational studies on a kind of novel energetic materials tetrahedrane and nitro derivatives[J].
J Mol Struct Theochem, 2004, 668: 189-195. DOI:10.1016/j.theochem.2003.10.054 |
| [5] |
Neutz J, Grosshardt O, Schaufele S, et al. Synthesis, characterization and thermal behaviour of guanidinium-5-aminotetrazolate(GA)-a new nitrogen-rich compound[J].
Propellants, Explos, Pyrotech, 2003, 28(4): 181-188. DOI:10.1002/(ISSN)1521-4087 |
| [6] |
Huynh M H V, Hiskey M A, Pollard C J, et al. 4, 4', 6, 6'-Tetra-substituted hydrazo-and zzo-1, 3, 5-triazines[J].
J Energ Mater, 2004, 22(4): 217-229. DOI:10.1080/07370650490893054 |
| [7] |
Churakov A M, Smimov O Y, Ioffe S L, et al. Benzo-1, 2, 3, 4-tetrazine 1, 3-dioxides:synthesis and NMR study[J].
Eur J Org Chem, 2002, 14: 2342-2349. |
| [8] |
Tartakovsky V A. The design of stable high nitrogen systems[J].
Mater Res Soc Symp Proc, 1996, 418: 15-24. |
| [9] |
Banert K, Joo Y H, Rüffer T, et al. The exciting chemistry of tetraazidomethane[J].
Angew Chem Int Ed, 2007, 46(7): 1168-1171. DOI:10.1002/(ISSN)1521-3773 |
| [10] |
Zheng W, Wong N B, Liang X, et al. Theoretical prediction of properties of triazidotri-s-triazine and its azido-tetrazole isomerism[J].
J Phys Chem, A, 2004, 108: 840-847. DOI:10.1021/jp037078x |
| [11] |
Huynh M H V, Hiskey M A, Archuleta J G, et al. 3, 6-Di(azido)-1, 2, 4, 5-tetrazine:a precursor for the preparation of carbon nanospheres and nitrogen-rich carbon nitrides[J].
Angew Chem Int Ed, 2004, 43: 5658-5661. DOI:10.1002/(ISSN)1521-3773 |
| [12] |
Huynh M H V, Hiskey M A, Chavez D E, et al. Synthesis, characterization, and energetic properties of diazido heteroaromatic high-nitrogen C—N compound[J].
J Am Chem Soc, 2005, 127: 12537-12543. DOI:10.1021/ja0509735 |
| [13] |
Huynh M H V, Hiskey M A, Hartline E L, et al. Polyazido high-nitrogen compounds:hydrazo-and azo-1, 3, 5-triazine[J].
Angew Chem Int Ed, 2004, 43(37): 4924-4928. DOI:10.1002/(ISSN)1521-3773 |
| [14] |
Chavez D E, Hiskey M A, Gilardi R D. 3, 3'-Azobis(6-amino-1, 2, 4, 5-tetrazine):a novel high-nitrogen energetic material[J].
Angew Chem Int Ed, 2000, 39(10): 1791-1793. DOI:10.1002/(SICI)1521-3773(20000515)39:10<1791::AID-ANIE1791>3.0.CO;2-9 |
| [15] |
李玉川, 李生华, 祁才, 等. 新型多氮化合物1, 1'-偶氮-1, 2, 3-三唑的合成与性能研究[J].
化学学报, 2011, 69(19): 2159-2165. Li Y C, Li S H, Qi C, et al. Synthesis and performance of a novel poly-nitrogen compound 1, 1'-azobis-1, 2, 3-triazole[J]. Acta Chim Sinica, 2011, 69(19): 2159-2165. |
| [16] |
Christoph J G, Lancaster P, Wilhelm J S, et al. Isocyanogen tetraazide and its preparation: US, 2990412[P], 1961.
|
| [17] |
Banert K, Richter S, Schaarschmidt D, et al. Well know or new synthesis and structure assignment of binary C2N14 compounds reinvestigated[J].
Angew Chem Int Ed, 2013, 52: 1-5. DOI:10.1002/anie.201209858 |
| [18] |
Klapötke T M, Martin F A, Stierstorfer J. C2N14:an energetic and highly sensitive binary azidotetrazole[J].
Angew Chem Int Ed, 2011, 50: 4227-4229. DOI:10.1002/anie.v50.18 |
| [19] |
Becke A D. Density-functional thermochemistry.Ⅲ.The role of exact exchange[J].
J Chem Phys, 1993, 98(7): 5648-5652. DOI:10.1063/1.464913 |
| [20] |
林梦海.
量子化学计算方法与应用[M]. 北京: 科学出版社, 2004.
|
| [21] |
Nicolaides A, Radom L. An evaluation of the performance of G2, G2(MP2) and G2(MP2, SVP) theories for heats of formation and heats of reaction in the case of "large" hydrocarbons[J].
Molecular Physics, 1996, 88(3): 759-765. DOI:10.1080/00268979609482452 |
| [22] |
Curtiss L A, Raghavachari K, Redfern P C, et al. Assement of gaussian-2 and density functional theories for the computation of enthalpies of formation[J].
J Chem Phys, 1997, 106(3): 1063 DOI:10.1063/1.473182 |
| [23] |
Byrd E F C, Rice B M. Improved prediction of heats of formation of energetic material using quantum chemical methods[J].
J Phys Chem A, 2006, 110(3): 1005-1013. DOI:10.1021/jp0536192 |
| [24] |
Rice B M, Pai S V, Hare J. Predicting heats of formation of energetic materials using quantum chemical calculation[J].
Comb Flame, 1999, 118(3): 445-458. DOI:10.1016/S0010-2180(99)00008-5 |
| [25] |
Ochterski J W, Petersson G A, Montgomery J A. A complete basis set model chemistry V.extension to six or more heavy atoms[J].
J Chem Phys, 1996, 204: 2598 |
| [26] |
Politzer P, Murray J S, Grice M E, et al. Calculation of heats of sublimation and solid phase heats of formation[J].
Mol Phys, 1997, 91: 923 DOI:10.1080/002689797171030 |
| [27] |
Kamlet M J, Jacobs S J. Chemistry of detonation Ⅰ.a simple method for calculating detonation properties of CHNO explosives[J].
J Chem Phy, 1968, 48(1): 23-25. DOI:10.1063/1.1667908 |
| [28] |
Cox J D, Wagman D D, Medvedev V A.
CODATA key values for thermodynamics[M]. New York: Hemisphere Publishing Corp, 1989.
|
| [29] |
ZHANG Xi-he, YUN Zhu-hui.
Explosive Chemistry[M]. Beijing: National Defence Industry Press, 1989.
|
| [30] |
MAN Tian-tian, NIU Xiao-qing, ZHANG Jian-guo, et al. Moleculardesign and theoretical study on novel high-nitrogen energetic azido compounds[J].
Chinese Journal of Energetic Materials, 2012, 20(5): 528-533. |
1-Diazidecarbonimidoyl-5-azidotetrazole(DACAT) was prepared via diazotized substitution reaction and cyclization reaction using triaminoguanidinium as raw material.Its structure was confirmed by IR, 13C NMR and 14N NMR.The influence of triaminoguanidinium/sodium nitrite molar ratio, reaction temperature, reaction time and pH of system on the yield of reaction was examined.The geometry of DACAT were optimized at the B3LYP/6-31G(d, p) basis set level using a density functional theory(DFT).Theoretical density, enthalpy of formation of gas phase, enthalpy of formation of solid phase, detonation velocity and detonation pressure for DACAT were calculated by Monte-Carlo method, complete base set method(CBS-4 M) and Kamlet-Jacobs formula, respectively.




