富氮化合物通常指含氮量达到50%以上的氮杂环类化合物, 包括五元氮杂环化合物(咪唑、吡唑、三唑、四唑)、六元氮杂环化合物(二嗪、三嗪、四嗪)及富氮呋咱等数种[1-3]。在含有氮氧配键的杂环化合物中, 呋咱并吡嗪类化合物受到各国的广泛关注[4-8], 其中呋咱并[3, 4-b]四唑并[1, 2-d]吡嗪类化合物是一类新型的富氮高能化合物, 其分子结构中含有大量的N—N、N—O和C—N键, 因而具有高的正生成焓, 且分子结构中的低碳、氢含量使其更容易达到氧平衡。7-叠氮基呋咱并[3, 4-b]四唑并[1, 2-d]吡嗪(AzFTP)和7-氨基呋咱并[3, 4-b]四唑并[1, 2-d]吡嗪(AmFTP)为该类型化合物中的代表, 其含氮量分别高达68.6%和62.9%, 可用于高能钝感炸药、气体发生剂、低特征信号推进剂和烟火药等[9]。以上化合物的制备反应条件简单, 收率高, 所用原料成本低廉, 易于实现工业化生产, 应用前景十分广阔。
Andrianov等[9]首次报道了AzFTP和AmFTP的合成, 表征了AzFTP的晶体结构, 但未对AmFTP的晶体结构及以上化合物的热性能进行进一步研究。为了更好地研究AzFTP和AmFTP的结构与其热稳定性的关系, 本研究以5, 6-二氯呋咱并[3, 4-b]吡嗪为原料, 经叠氮化、胺化反应分别制备了AzFTP和AmFTP, 并完善了两种化合物的结构表征数据; 首次培养出AmFTP的单晶, 并进行了晶体结构研究; 初步研究了AzFTP和AmFTP的热性能, 为进一步开展其应用奠定基础。
2 实验部分 2.1 试剂与仪器5, 6-二氯呋咱并[3, 4-b]吡嗪由实验室自制[10]; 叠氮化钠, 氨水(25% aq.), 丙酮, 二氯甲烷, 石油醚(60~90 ℃), 乙酸乙酯均为分析纯; 乙腈为色谱纯。
ZF-Ⅱ型三用紫外仪, 上海市安亭电子仪器厂; NEXUS 870型傅里叶变换红外光谱仪, 美国热电尼高力公司; AV 500型(500MHz)超导核磁共振仪, 瑞士BRUKER公司; micrOTOF-Q Ⅱ型质谱仪, 美国BRUKER公司; VARIO-EL-3型元素分析仪, 德国EXEMENTAR公司; LC-2010A型高效液相色谱仪(归一化法), 日本岛津公司; Q-200型差示扫描量热仪, 美国TA公司; TA 2950热重仪, 美国Nicolet公司; X-6型显微熔点测定仪, 北京泰克仪器有限公司。
2.2 合成路线|
|
图 Scheme 1 |
将叠氮化钠(3.12 g, 48 mmol)溶于水(20 mL)中, 搅拌下向其中滴加5, 6-二氯呋咱并[3, 4-b]吡嗪(3.06 g, 16 mmol)的丙酮(10 mL)溶液, 约10 min滴毕, 继续在室温下搅拌反应2 h。停止反应, 用二氯甲烷(3×30 mL)萃取, 合并有机相并用饱和食盐水洗涤, 经无水硫酸钠干燥后蒸除溶剂, 得7-叠氮基呋咱并[3, 4-b]四唑并[1, 2-d]吡嗪3.05 g, 收率93.4%, m.p.: 97 ℃。
13C NMR (DMSO-d6, 125 MHz), δ: 154.14, 152.46, 143.21, 141.08; IR (KBr, ν/cm-1): 2188 (N3), 1642, 1516 (C=N), 1493, 1411, 1305, 1214, 994 (呋咱环), 967, 864, 621; Anal. Calcd for C4N10O: C 23.54, N 68.62; Found C 23.58, N 68.42。
2.3.2 7-氨基呋咱并[3, 4-b]四唑并[1, 2-d]吡嗪(AmFTP)的合成将AzFTP(2.04 g, 10 mmol)溶于无水乙腈(60 mL)中, 搅拌下向其中滴加25%氨水(1.4 mL), 约10 min滴毕, 继续在室温下搅拌反应0.5 h。停止反应, 过滤除去不溶物, 所得滤液蒸除溶剂后经柱色谱分离(洗脱剂为石油醚:乙酸乙酯= 2:1), 得7-氨基呋咱并[3, 4-b]四唑并[1, 2-d]吡嗪1.55 g, 收率87.1%, m.p.: 186 ℃(分解)。
1H NMR (DMSO-d6, 500 MHz), δ: 9.22 (d, 2H, NH2); 13C NMR (DMSO-d6, 125 MHz), δ: 154.38, 151.01, 142.70, 140.44; IR (KBr, ν/cm-1): 3309, 3160 (—NH2), 1672, 1551, 1519(C=N), 1423, 1332, 1230, 1123, 1081, 1007(呋咱环), 973, 850; Anal. Calcd for C4H2N8O: C 26.97, H 1.13, N 62.91; Found C 26.69, H 1.18, N 63.00。
2.4 AmFTP的单晶培养与测定 2.4.1 AmFTP单晶培养称取0.2 g自制AmFTP纯品, 加入适量丙酮, 充分溶解后得到淡黄色溶液, 置于干净的试管中, 30 ℃下放置3 d后, 得到淡黄色晶体。从中挑选适当大小的晶体颗粒进行结构测试及分析。
2.4.2 AmFTP结构测定选取尺寸为0.36 mm×0.28 mm×0.14 mm的单晶, 在Siemens P4型四圆衍射仪上, 用Mo Kα射线(λ=0.071073 nm)、石墨单色器, 在296(2) K温度下, 以ω扫描方式扫描, 扫描范围: 3.05°≤θ≤25.09°, -5≤h≤8, -8≤k≤9, -13≤ l ≤14, 共收集衍射点3343个, 其中独立衍射点1219个[R(int)=0.0536], 选取l>2σ(l)的1219个点用于结构的测定和修正, 结构参数经全矩阵最小二乘法修正, 所有计算工作均用SHELXTL097程序包完成。CCDC: 955442。
3 结果与讨论 3.1 AmFTP的晶体结构分析AmFTP晶体的分子结构和分子在晶胞中的堆积分别示于图 1和图 2, 晶体结构数据及精修参数、主要键长和键角分别列于表 1和表 2中。

|
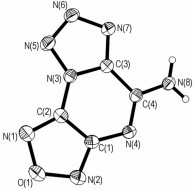
图 1 AmFTP的分子立体构型图 Fig.1 Spatial configuration of AmFTP 7-aminofurazano[3, 4-b]tetrazolo[1, 2-d]pyrazine |
|
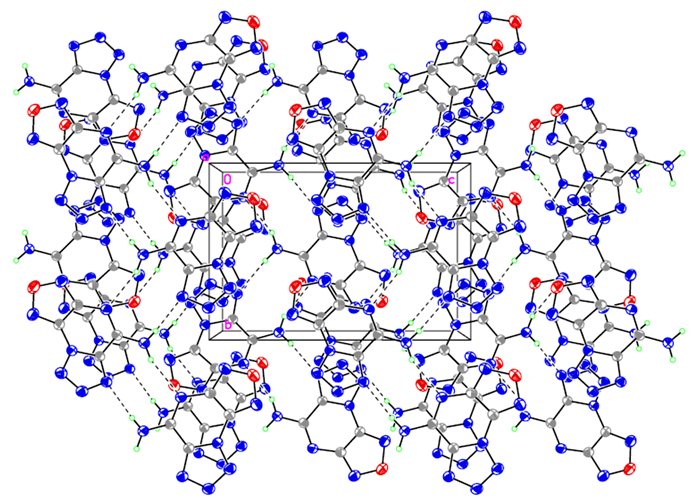
图 2 AmFTP的晶胞堆积图 Fig.2 Unit cell diagram of AmFTP |
| 表 1 AmFTP的晶体结构数据及精修参数 Tab.1 Crystal structure refinement parameters of AmFTP |
| 表 2 AmFTP的氢键参数 Tab.2 H-bonding parameters of AmFTP |
分析图 1和表 2可知, 氨基氮同相连的吡嗪环碳原子之间的N(8)—C(4)键长为1.318(2)Å, 接近C=N键长[11], 表明氨基同吡嗪环存在一定程度的共轭。除N(8)—C(4)外, 其余C—N键长从1.293(3)Å到1.387(3)Å不等, 平均键长1.33Å[11], 所有键长均介于报道的C—N单键与C=N双键键长之间; 二面角N(2)—C(1)—C(2)—N(3)、N(7)—C(3)—C(4)—N(4)和N(5)—N(3)—C(2)—N(1)分别为179.52(19)°、179.4(2)°和-0.5(4)°, 说明呋咱环、吡嗪环和四唑环均处在一个平面内, 形成了一个完整的共轭体系, 使得该化合物表现出较好的稳定性。
AmFTP的氢键数据如表 3。从图 2可以看出, AmFTP分子间排列成规则的层状结构, 从表 3可知, AmFTP分子间存在两种分子间氢键: (1)氨基上的氢与相邻分子四唑环上氮原子之间的氢键, 即N(8)—H(8A)…N(7), 其键长为2.1669(17)Å; (2)氨基上的氢与相邻分子吡嗪环上氮原子之间的氢键, 即N(8)—H(8B)…N(4), 其键长为2.2009(16)Å。这两种氢键连接相邻的分子, 使得分子排列更加紧密, 进而使晶体结构更加稳定。
| 表 3 AmFTP的氢键参数 Tab.3 H-bonding parameters of AmFTP |
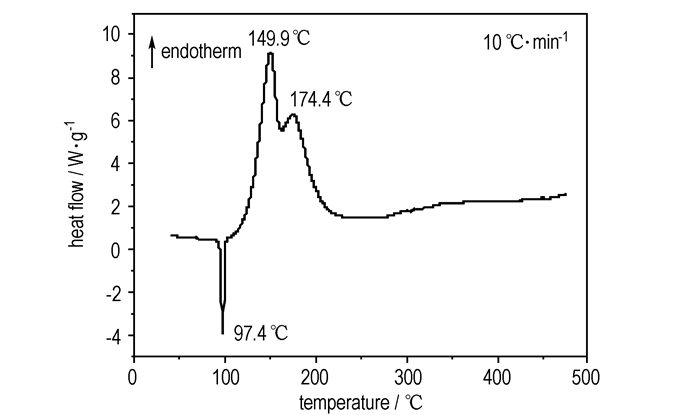
AzFTP在升温速率为10 ℃·min-1下的DSC曲线如图 3所示。由图 3可见,AzFTP有3个明显的吸热、放热峰, Tp1=97.4 ℃时的尖锐吸热峰为该物质的熔化峰, 显示为该物质的熔点; Tp2=149.9 ℃时的放热峰为该物质的第一个热分解放热峰, Tp3=174.4 ℃时的放热峰为该物质的第二个热分解放热峰。
|
图 3 AzFTP的DSC曲线 Fig.3 DSC curve of AzFTP |
图 4为AzFTP在常压下的TG/DTG曲线, 从图 4中可以看出该试样的热分解分为两个阶段。在温度低于134.96 ℃时, 该物质失重较少, 累积失重仅为6.9%;失重第一阶段的峰值出现在148.7~241.4 ℃, 累积失重为39.3%;失重第二阶段为一持续过程, 无明显峰值, 至497.84 ℃时热分解累计失重3.8%。对比DSC与TG/DTG分析结果, 其DTG峰值温度与DSC热分解第一个放热峰一致。DSC曲线上97.4 ℃的吸热峰是该物质的熔融吸热过程。因此, DSC曲线上的放热峰和DTG曲线上的失重峰均为该物质的液相分解过程。

|
图 4 AzFTP的TG-DTG曲线 Fig.4 TG-DTG curves of AzFTP |
AmFTP在升温速率为10 ℃·min-1下的DSC曲线如图 5所示。在图 5上未观察到AmFTP的吸热峰, 在Tp=186.0 ℃的尖锐放热峰为该物质的热分解放热峰, 说明AmFTP未达到熔点即开始分解。

|
图 5 AmFTP的DSC曲线 Fig.5 DSC curve of AmFTP |
图 6为AmFTP在常压下的TG/DTG曲线, 从图 6中可以看出, 当温度低于181.5 ℃时该物质失重较少, 累积失重仅为4.4%;在温度从181 ℃上升到188 ℃的过程中, 该物质快速失重, 热分解累计失重达85.2%。对比DSC与TG/DTG分析结果, 其DTG峰值温度与DSC热分解放热峰一致。由于DSC曲线上未出现吸热熔化峰, 因此DSC的放热峰和DTG的失重峰均为该物质的固相分解过程。

|
图 6 AmFTP的TG-DTG曲线 Fig.6 TG-DTG curves of AmFTP |
对比AzFTP和AmFTP的热分析结果发现, AmFTP的热稳定性好于AzFTP。这是由于AmFTP分子中的氨基氢与相邻分子形成氢键, 提高了分子的晶格能, 使得其熔点升高, 热稳定性增强; 而AzFTP分子中无氢键作用, 晶格能较低, 且叠氮基不稳定, 加热易分解释放N2, 故AzFTP的熔点和分解点较AmFTP低。
4 结论以5, 6-二氯呋咱并[3, 4-b]吡嗪为原料, 经叠氮化、氨化反应合成了7-叠氮基呋咱并[3, 4-b]四唑并[1, 2-d]吡嗪(AzFTP)和7-氨基呋咱并[3, 4-b]四唑并[1, 2-d]吡嗪(AmFTP), 收率分别高达93.4%和87.1%。
首次培养了AmFTP单晶, X射线单晶衍射结果表明: AmFTP晶体属于正交晶系, P212121空间群, a=0.7117(18) nm, b=0.8088(2) nm, c=1.1871(8) nm, V=0.6833(3) nm3, Z=4, Dc=1.732 g·cm-3, μ=0.138 mm-1, F(000)=360, R1=0.0376, wR2=0.0988。AmFTP分子间氢键连接相邻的分子构成二维层状结构, 使得分子排列规则, 晶体结构更稳定。
分析了AzFTP和AmFTP的热稳定性, 其热分解峰温分别为149.9, 186.0 ℃, 表明AmFTP比AzFTP具有更好的热稳定性。
| [1] |
黄明, 李洪珍, 李金山. 高氮含能化合物的合成及反应性[J].
含能材料, 2006, 14(6): 457-462. HUANG Ming, LI Hong-zhen, LI Jin-shan. Review on synthesis of high-nitrogen energetic compouds[J]. Chinese Journal of Energetic Materials(Hanneng Cailiao), 2006, 14(6): 457-462. |
| [2] |
张德雄, 张衍, 王琦. 呋咱系列高能量密度材料的发展[J].
固体火箭技术, 2004, 27(1): 32-36. ZHANG De-xiong, ZHANG Yan, WANG Qi. Advances in high energy density matter of furazan series[J]. Journal of Solid Rocket Technology, 2004, 27(1): 32-36. |
| [3] |
王宏社, 杜志明. 富氮化合物研究进展[J].
含能材料, 2005, 13(3): 196-199. WANG Hong-she, DU Zhi-ming. Progress in synthesis and properties of nitrogen-rich compounds[J]. Chinese Journal of Energetic Materials(Hanneng Cailiao), 2005, 13(3): 196-199. |
| [4] |
Sheremetev A B, Yudin I L. Advances in the chemistry of furazano[3, 4-b]pyrazines and their analogues[J].
Russia Chemical Reviews, 2003, 72(1): 87-100. DOI:10.1070/RC2003v072n01ABEH000776 |
| [5] |
Tselinskii I V, Mel′nikova S F, Romanova T V, et al. 4H, 8H-Difurazano[3, 4-b:3′, 4′-e]pyrazine and some its derivatives[J].
Russia Journal of Organic Chemistry, 1997, 33(11): 1656-1665. |
| [6] |
Starchenkov I B, Andrianov V G, Mishnev A F. Chemistry of furazano[3, 4-b]pyrazine. 1. Synthesis and thermodynamic appraisal of 4, 8-dihydrodifurazano[3, 4-b]pyrazine and its derivatives[J].
Chemistry of Heterocyclic Compounds, 1997, 33(2): 21-6228. |
| [7] |
毕福强, 王伯周, 王锡杰, 等. 1, 4-二硝基呋咱并[3, 4-b]哌嗪(DNFP)的合成[J].
含能材料, 2009, 17(5): 537-540. BI Fu-qiang, WANG Bo-zhou, WANG Xi-jie, et al. Synthesis of 1, 4-dinitrofurazano[3, 4-b]piperazine[J]. Chinese Journal of Energetic Materials(Hanneng Cailiao), 2009, 17(5): 537-540. |
| [8] |
刘宁, 王伯周, 李辉, 等. 1, 2, 3-三氮唑[4, 5-e]呋咱并[3, 4-b]吡嗪-6-氧化物的合成与表征[J].
兵工学报, 2012, 33((增刊2)): 88-91. LIU Ning, WANG Bo-zhou, LI Hui, et al. Synthesis and characterization of 1, 2, 3-triazolo[4, 5-e]furazano[3, 4-b]pyrazine-6-oxides[J]. Acta Armamenterii, 2012, 33((Suppl. 2): 88-91. |
| [9] |
Starchenkov I B, Andrianov V G, Mishnev A F. . Chemistry of furazano[3, 4-b]pyrazines 2.nucleophilic substitution of the azido group in furazano[3, 4-b]pyrazines[J].
Chemistry of Heterocyclic Compounds, 1997, 33(8): 977-981. DOI:10.1007/BF02253173 |
| [10] |
Starchenkov I B, Andrianov V G. Chemistry of furazano[3, 4-b]pyrazines 3. method for the synthesis of 5, 6-disubstituted furazano[3, 4-b]pyrazines[J].
Chemistry of Heterocyclic Compounds, 1997, 33(10): 1219-1233. DOI:10.1007/BF02290874 |
| [11] |
陈小明, 蔡继文, 编著.
单晶分析结构原理及实践[M]. 北京: 科学出版社, 2003: 124-126.
|
7-Azidofurazano[3, 4-b]tetrazolo[1, 2-d]pyrazine(AzFTP) and 7-aminofurazano[3, 4-b]tetrazolo[1, 2-d]pyrazine (AmFTP) were synthesized using 5, 6-dichlorofurazano[3, 4-b]pyrazine as starting material, via azidation and amination reaction. The single crystal of AmFTP was firstly cultivated and tested by single-crystal X-ray diffraction.



