笼状烃分子具有高环张力和高碳氢比, 因而具有高密度、高体积燃烧热, 如五环[5.4.0.02, 6.03, 10. 05, 9]十一烷类化合物, 密度>1.2 g·cm-3, 燃烧热>50 MJ·L-1, 可用作高能燃料或炸药组分, 通过提高燃料或炸药的燃烧热或爆热来提高综合性能和毁伤威力, 受到燃料研究者的普遍关注[1-4]。由于笼状碳氢化合物的熔点高, 挥发性强, 在应用体系中易迁移, 一定程度上限制了其应用。
笼状烃的衍生物可在提高化合物能量密度的同时, 改善笼状烃的挥发性能, 具有高燃烧热及爆热[5]。本研究以五环[5.4.0.02, 6.03, 10. 05, 9]十一烷、甲基五环[5.4.0.02, 6.03, 10. 05, 9]十一烷为母体结构, 合成了高张力笼状烃衍生物, 通过羰基的反应在分子中引入硝基等含能基团, 可用作新型炸药或高能燃料组分, 用于提高炸药爆热或高能燃料的燃烧热。
2 实验部分 2.1 试剂与仪器2, 4-二硝基苯肼、苯肼、水合联氨、乙醇等均为分析纯; 环戊二烯(CPD)、甲基环戊二烯(MCPD)分别由双环戊二烯、甲基环戊二烯二聚体170 ℃下分解制得, 纯度大于98%。
美国惠普公司HP 5989B型有机质谱仪; 上海海欣色谱仪器有限公司GC-930型气相色谱仪; 美国Nicolet公司Nexus 870型傅里叶变换红外光谱仪; 美国Varian公司500MHz INOVA核磁共振波谱仪; 北京汇亿鑫电光源技术开发有限公司1000 W高压汞灯。
2.2 实验过程 2.2.1 合成路线合成路线如Scheme 1所示。
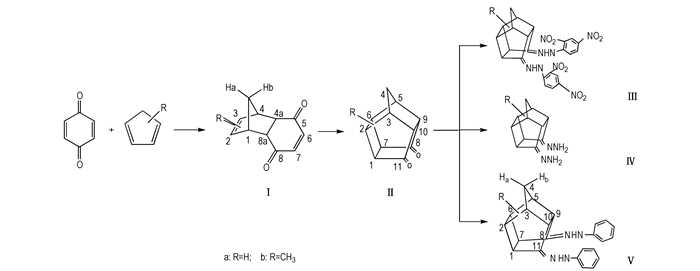
|
Scheme1 Synthesis of title compound |
48.9 g苯醌溶于500 mL无水乙醇, 冰盐浴中搅拌2h, 冷却至-4 ℃。30 g新蒸的CPD溶于100 mL乙醇, 缓慢滴加至上述溶液中, 搅拌, 混合物逐渐升至室温, 继续搅拌5 h, 停止, 蒸除溶剂, 粗产物乙醇重结晶得棕色晶体, m.p. 65~66 ℃, 收率92.1%。MS: m/z: 174(M+), 108, 66。IR(KBr, ν/cm-1): 2944, 2875, 1670, 1604, 1454, 1336, 1234。1H NMR(CDCl3), δ: 1.43(d, 1H, Ha), 1.55(s, 1H, Hb), 3.22(s, 2H, H1, H4), 3.55(s, 2H, H4α, H8α), 6.07(s, 2H, H2, H3), 6.57 (s, 2H, H6, H7)。13C NMR(CDCl3), δ: 48.31(CH, C1, C4), 48.66(C, C1, C8α), 48.71(CH2, 桥上CH2), 135.27(CH, C2, C3), 142.01 (CH, C6, C7), 199.35(C, C5, C8)。
2.2.3 五环[5.4.0.02, 6.03, 10.05, 9]十一烷-8, 11-二酮的合成(Ⅱa, R=H)20 g endo-1, 4, 4α, 8α-四氢-1, 4-亚甲基萘-5, 8-二醌溶于300 mL乙酸乙酯, 反应液置于石英烧瓶中, 高压汞灯光照下回流24 h, 蒸除溶剂, 粗产物乙酸乙酯重结晶得浅棕色晶体, m.p. 162~164 ℃, 收率81.0%。MS: m/z: 174 (M+)。IR(KBr, ν/cm-1): 2977, 2954, 2868, 1762, 1728, 1456, 1176。
2.2.4 五环[5.4.0.02, 6.03, 10.05, 9]十一烷-8, 11-二酮-2, 4-二硝基苯腙的合成(Ⅲa, R=H)0.5 g 2, 4-二硝基苯肼中加入2 mL浓硫酸, 搅拌, 固体溶解后加入10 mL 95%乙醇, 0.3 g五环[5.4.0.02, 6.03, 10.05, 9]十一烷-8, 11-二酮溶于10 mL乙醇滴加至上述体系中, 反应30 min后过滤, 氯仿重结晶得橙红色固体, m.p. 125~127 ℃, 收率93.0%。MS: m/z: 277, 183。IR(KBr, ν/cm-1): 3430, 3106, 2977, 2862, 1618, 1594, 1504, 1518, 1337, 886, 851。
2.2.5 五环[5.4.0.02, 6.03, 10.05, 9]十一烷-8, 11-二酮-腙的合成(Ⅳa, R=H)1.0 g五环[5.4.0.02, 6.03, 10.05, 9]十一烷-8, 11-二酮溶于10 mL乙醇, 搅拌下滴加至0.3 g水合联氨中, 室温反应3 h, 过滤, 粗产品氯仿重结晶得白色固体, m.p. 234~251 ℃, 收率40.2%。IR(KBr, ν/cm-1): 3426, 2966, 2864, 1454, 1640, 1300, 765。
2.2.6 五环[5.4.0.02, 6.03, 10.05, 9]十一烷-8, 11-二酮-苯腙的合成(Ⅴa, R=H)0.5 g苯肼溶于10 mL无水乙醇, 搅拌下滴加0.4 g五环[5.4.0.02, 6.03, 10.05, 9]十一烷-8, 11-二酮的乙醇溶液, 室温反应4 h, 过滤, 粗产品氯仿重结晶得白色固体, m.p. 101~103 ℃, 收率61.2%。MS: m/z: 354(M+), 247, 156。IR(KBr, ν/cm-1): 3347, 3270, 3027, 2970, 2865, 1738, 1603, 1498, 747, 694。1H NMR(CDCl3), δ: 1.60(m, 2H, H3, H5), 1.94(m, 1H, Ha), 2.66(m, 2H, H2, H6), 2.92~3.47(m, 4H, H9, H10, H1, H7), 3.62(s, 1H, Hb), 6.50~7.10(m, 10H, 芳环上H), 7.14~7.18(m, 2H, NH)。
2.2.7 甲基-endo-1, 4, 4α, 8α-四氢-1, 4-亚甲基萘-5, 8-二醌的合成(Ⅰb, R=CH3)21.6 g苯醌溶于100 mL无水乙醇, 冰浴搅拌2 h, 15.6 g新蒸MCPD溶于100 mL乙醇, 缓慢滴加至上述溶液中, 混合物逐渐升至室温, 继续反应10 h, 反应结束后蒸除溶剂, 粗产物乙醇重结晶得浅棕色晶体, m.p. 52~54 ℃, 收率94.1%。MS: m/z: 188(M+), 80。IR(KBr, ν/cm-1): 3438, 3051, 2962, 2930, 2868, 1665, 1606, 1379, 864, 734。1H NMR(CDCl3), δ: 1.38(m, 1H, , Ha), 1.45~1.74(m, 3H, CH3), 2.86(d, 1H, Hb), 3.21~3.24(m, 1H, H4), 3.33~3.36(m, 1H, H4α), 3.44-3.47(m, 1H, H8α), 5.60~6.00(m, 2H, H2, H3), 6.51~6.57 (m, 2H, H6, H7)。
2.2.8 甲基五环[5.4.0.02, 6.03, 10.05, 9]十一烷-8, 11-二酮的合成(Ⅱb, R=CH3)10 g甲基-endo-1, 4, 4α, 8α-四氢-1, 4-亚甲基萘-5, 8-二醌溶于400 mL乙酸乙酯, 反应液于石英烧瓶中, 高压汞灯光照下回流28 h, 蒸除溶剂, 粗产物乙酸乙酯重结晶得浅棕色晶体, m.p. 95~97 ℃, 收率78.0%。IR(KBr, ν/cm-1): 3444), 2971, 2925, 2864, 1750, 1377。1H NMR(CDCl3), δ:1.222(s, 3H, CH3), 1.815, 1.838, 1.970, 1.993 (AB, JAB=11.5Hz, H4a, H4b), 2.47(m, 1H, H6), 2.80~2.86(m, 5H, H1, H2, H3, H9, H10), 3.257(m, 1H, H7)。13C NMR(CDCl3), δ: 16.12(CH3), 39.99(C3), 43.33(C2), 44.56 (C6), 44.57(C7), 44.77(C10), 46.33(C4), 52.83(C5), 55.83(C1), 60.34(C9), 211.47(C8), 212.17(C11)。
2.2.9 甲基五环[5.4.0.02, 6.03, 10.05, 9]十一烷-8, 11-二酮-2, 4-二硝基苯腙的合成(Ⅲb, R=CH3)0.5 g 2, 4-二硝基苯肼中加入2 mL浓硫酸, 溶解后加入10 mL 95%乙醇, 搅拌, 滴加0.4 g甲基五环[5.4.0.02, 6.03, 10.05, 9]十一烷-8, 11-二酮的乙醇溶液, 室温反应2 h后过滤, 粗产品氯仿重结晶, m.p. 132~133 ℃, 收率77.6%。MS: m/z: 368。IR(KBr, ν/cm-1): 3436, 2964, 2867, 1618, 1338。
2.2.10 甲基五环[5.4.0.02, 6.03, 10.05, 9]十一烷-8, 11-二酮-腙的合成(Ⅳb, R=CH3)0.2 g甲基五环[5.4.0.02, 6.03, 10.05, 9]十一烷-8, 11-二酮溶于10 mL乙醇, 搅拌下滴加至0.3 g水合联氨中, 45 ℃反应4 h后过滤, 粗产品氯仿重结晶得白色固体, m.p. 215~217 ℃, 收率31.3%。IR(KBr, ν/cm-1): 3232, 2960, 2862, 1633, 1455, 1330。
2.2.11 甲基五环[5.4.0.02, 6.03, 10.05, 9]十一烷-8, 11-二酮-苯腙的合成(Ⅴb, R=CH3)0.5 g苯肼溶于10 mL无水乙醇中, 搅拌, 滴加0.4 g甲基五环[5.4.0.02, 6.03, 10.05, 9]十一烷-8, 11-二酮的乙醇溶液, 室温反应4 h, 过滤, 粗产品氯仿重结晶得白色固体, m.p. 105~107 ℃, 收率51.3%。MS: m/z: 368(M+), 261。IR(KBr, ν/cm-1): 3429, 3052, 2952, 2864, 1602, 1502, 1258, 749, 693。
3 结果与讨论研究了部分笼状烃衍生物的热分解行为, 并与五环[5.4.0.02, 6.03, 10.05, 9]十一烷(PCUD)的热分解行为进行了对比, 选取了含硝基的衍生物五环[5.4.0.02, 6.03, 10.05, 9]十一烷-8, 11-二酮-2, 4-二硝基苯腙(Ⅲa)和不含硝基的五环[5.4.0.02, 6.03, 10.05, 9]十一烷-8, 11-二酮-苯腙(Ⅴa)、甲基五环[5.4.0.02, 6.03, 10.05, 9]十一烷-8, 11-二酮-苯腙(Ⅴb), 各化合物在不同压力下DSC曲线如图 1所示。随着压力的增大, 笼状烃衍生物分解峰的峰值温度略有升高, 五环[5.4.0.02, 6.03, 10.05, 9]十一烷-8, 11二酮-2, 4-二硝基苯腙在137℃处为熔化吸热峰, 258 ℃和282 ℃处为分解放热峰。五环[5.4.0.02, 6.03, 10.05, 9]十一烷-8, 11-二酮-苯腙和甲基五环[5.4.0.02, 6.03, 10.05, 9]十一烷-8, 11-二酮-苯腙的DSC曲线类似且都包含多个放热峰, 说明笼上的烷基取代基对化合物热分解性能影响较小, 两种化合物在高温下均为分步分解。五环[5.4.0.02, 6.03, 10.05, 9]十一烷-8, 11二酮-2, 4-二硝基苯腙中芳环上硝基的吸电子作用强, 碳氮双键比五环[5.4.0.02, 6.03, 10.05, 9]十一烷-8, 11二酮-苯腙中的弱, 分解步骤较少。
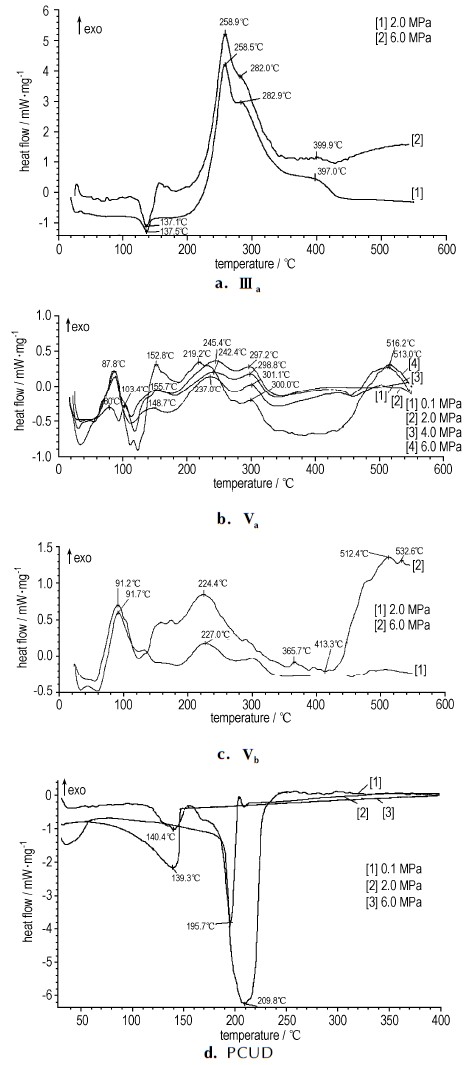
|
图 1 五环[5.4.0.02, 6.03, 10.05, 9]十一烷及衍生物Ⅲa, Ⅴa, Ⅴb的DSC曲线 Fig.1 DSC curves of pentacyclo[5.4.0.02, 6.03, 10.05, 9]undecane and derivatives Ⅲa, Ⅴa and Ⅴb |
高张力笼状烃衍生物的热分解行为与高张力笼状烃具有明显差异, 图 1d中五环十一烷为吸热分解, 且在加热下有明显的挥发过程, 增大压力挥发过程受到明显抑制; 笼状烃衍生物为放热分解, 且未见挥发现象, 说明笼状烃分子中引入其它含杂原子基团改善了分子的挥发性能, 且分子中引入吸电子基团后分解温度升高。
4 结论(1) 分别以环戊二烯和甲基环戊二烯为原料, 经过三步反应合成了五环[5.4.0.02, 6.03, 10. 05, 9]十一烷及甲基五环[5.4.0.02, 6.03, 10.05, 9]十一烷的腙、苯腙及2, 4-二硝基苯腙。
(2) 热分析结果表明, 高张力笼状烃腙类衍生物高温分步放热分解, 且分解温度随压力增大略有升高。五环[5.4.0.02, 6.03, 10. 05, 9]十一烷与其腙类衍生物的热分析结果对比可以看出, 高张力笼状烃结构中引入取代基后, 改善了笼状结构的挥发性, 热分烃解反应由吸热分解改变为放热分解。
| [1] |
邢恩会, 米镇涛, 张香文. 用作新型高密度燃料的高张力笼状烃的研究进展[J].
火炸药学报, 2004, 27(2): 13-16. XING En-hui, MI Zhen-tao, ZHANG Xiang-wen. Development of high strained caged hydrocarbons used as high density fuels[J]. Chinese Journal of Explosives & Propellants, 2004, 27(2): 13-16. |
| [2] |
Marchand A P. Synthesis and Chemistry of homocubanes, bishomocubanes, and trishomocubanes[J].
Chemical Review, 1989, 89(2): 1011-1036. |
| [3] |
邱丽美, 侯俊先, 韦伟, 等. 笼状碳氢化合物五环[5.4.0.02, 6.03, 10.05, 9]十一烷的密度泛函理论研究[J].
化学学报, 2008, 669(7): 745-750. QIU Li-mei, Hou Jun-xian, WEI Wei, et al. Density Functional Theory Investigation on a Caged Compound-Pentacyclo[5.4.0.02, 6.03, 10.05, 9]undecane[J]. Acta Chim Sinica, 2008, 669(7): 745-750. |
| [4] |
Martins F J C, Vujoen A M, Venter H J, et al. Synthesis of novel tetracyclo [6.3.0.02, 6.03, 10] undecane and tetracyclo[6.4.0.02, 6.03, 10]dodecane derivatives[J].
Tetrahedron, 1997, 53(44): 14991 DOI:10.1016/S0040-4020(97)01050-8 |
| [5] |
敬林, 李加荣, 史大昕, 等. 笼状碳氢燃料的研究进展[C]//中国化学会第五届全国化学推进剂会议, 2011年9月, 大连.
JING Lin, LI Jia-rong, SHI Da-xin, et al. Development of Caged Hydrocarbon Fuels[C]//The 5th Chemical Propellant Conference of Chinese Chemical Society, September 2011, Dalian. |
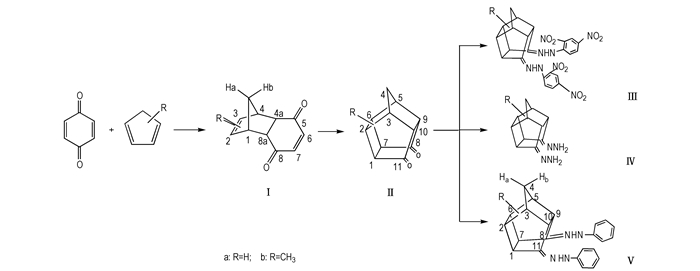
Derivatives of pentacyclo[5.4.0.02, 6.03, 10.05, 9]undecane or methylpentacyclo [5.4.0.02, 6.03, 10. 05, 9]undecane were synthesized and characterized by MS, IR and NMR. The thermal decomposition properties of some compounds were studied and compared with high caged hydrocarbon by PDSC.



