2. 中国工程物理研究院研究生部, 四川 绵阳 621900
2. Graduate School of CAEP, Mianyang 621900, China
多晶型现象[1]是炸药研究的一个重要方面,不同晶型炸药的性质各有差异(如感度、爆轰性能等),而这些性质对炸药的应用非常重要,因此研究多晶型炸药的性质及其重结晶具有重要意义。六硝基六氮杂异伍兹烷(HNIW,CL-20)作为现有能量最高的单质炸药已被广泛研究[2-4],但高成本和高感度限制了其广泛应用。CL-20在常温常压下稳定存在α-、β-、γ-及ε-四种晶型,其中ε-CL-20的密度最大[5],约为2.04 g·cm-3,热稳定性最好,感度也最低,在武器装备中应用的均为ε-CL-20。而通常硝解制得的是α-CL-20或γ-CL-20或二者的混合物[6-7],需通过转晶才能得到ε-CL-20,一般采用的是溶剂重结晶法[8]。但该法得到的ε-CL-20仍含有少量其它晶型(如α-、β-或γ-),使CL-20的密度降低,感度增加,由此也会影响炸药的爆轰性能[9]。因此,需要优化重结晶条件,以提高ε-CL-20的晶型纯度。此外,当CL-20炸药与溶剂接触或环境条件(温度或压力)改变时,也可导致晶型转变而降低密度,使炸药体积膨胀并产生裂纹,该缺陷裂纹可作为爆炸热点并敏化炸药,降低炸药的安全性及安定性[10-11]。
因此,考察CL-20的重结晶条件,控制晶型转变过程,不仅可以制得晶型纯度较高的ε-CL-20,提高炸药的密度; 还有助于改善CL-20的晶体质量,获得近似球形晶体,以降低感度,使其具有更广泛的应用[12]。而目前,关于CL-20的研究大多集中在改进合成方法、获得所需晶体和探索热分解机理等方面,为了掌握CL-20的晶型转变机理并制备晶型纯度较高的ε-CL-20,本文主要对CL-20的各种晶型、重结晶方法及晶型转变研究进展进行了综述。
2 CL-20的多晶型现象 2.1 CL-20各种晶型及结构CL-20是一种具有笼形结构的高能硝胺化合物,六个桥氮原子上各有一个硝基,不同的硝基取向、晶格堆积方式使其具有多种晶型,主要为α-、β-、γ-、ε-及ζ,晶体学数据及分子构型如表 1所示[7, 13, 16]。从分子构型来看,α-和γ-晶型属于非对称结构,而β-、ε-和ζ-晶型为对称结构。CL-20分子内原子位置对称与否,会影响分子电荷密度分布,造成表观的晶体偶极矩不同。α-和γ-CL-20具有相同的分子构型,只是晶胞的堆积方式不同而已,通常制得的α-CL-20为含H2O加合物,其中H2O能稳定α-CL-20且在晶胞空腔的占据率为17%~50%。将α-CL-20加热到100 ℃数小时即可脱水得到无水α-CL-20,但该无水α-晶体不能直接合成。用DSC研究α-CL-20的热稳定性时发现[14],在接近其分解温度时有δ-CL-20存在,但该晶体极不稳定,还未成功分离和鉴定结构。γ-CL-20在高于0.7 MPa压力下缓慢转变为ζ-CL-20[15],该ζ-晶体在常温常压下不稳定,但已成功测定其在高压下的结构[16]。根据不同晶型CL-20结构的差异性,可用X射线衍射(XRD)或红外光谱(FTIR)鉴定CL-20的晶型,并且通过特征峰的拟合计算进行相的定量分析。
2.2 CL-20各种晶型的稳定性CL-20重结晶时的晶型转变过程与不同晶型CL-20的热稳定性有密切关联,热稳定性越高的晶型在重结晶时越容易形成。通常Gibbs自由能越大的晶型,其热稳定性越低。若两种晶型在某温度下具有相同的Gibbs自由能,则其热稳定性相同,该温度称为晶型转变的临界点[17]。
Kholod等[18]用密度泛函理论研究不同构型CL-20分子的稳定性及转变机理发现,不同构型间转变的活化能很低且较接近,为5.0~16.7 kJ·mol-1。因此,CL-20分子发生构型转变所需的能量较少,而由此形成的不同晶型CL-20的转变能垒也较低,导致CL-20在重结晶时易发生晶型转变。
Foltz等[13]根据溶解速率、Russell等[15]基于DSC方法以及Sorescu等[19]从晶格能角度分别考察了不同晶型CL-20的稳定性,不同的研究方法得到的稳定性顺序不一致,分别为ε->γ->α-(有水)>β-,α-(有水) >ε->α-(无水) >β->γ-和ε->β->γ-。其原因是Foltz等考察的是CL-20在溶剂中溶解的热力学稳定性,而Russell等研究的是固相CL-20在加热条件下的热稳定性,即这两种测试方法研究的稳定性的概念不一样,也说明了CL-20晶型转变及稳定性的复杂性。在上述不同的稳定性顺序中,无水时ε-晶型都是最稳定的。但在常压下将CL-20固体不断加热时,α-、β-和ε-CL-20均可转变为γ-CL-20[15],即高温时γ-CL-20变为稳定晶型,说明不同晶型CL-20的稳定性顺序与温度有关。
2.3 CL-20各种晶型的物化性能CL-20与很多常用的炸药和粘结剂(如黑索今(RDX)、奥克托今(HMX)、太安(PETN)、硝酸酯、异氰酸酯及聚叠氮缩水甘油醚(GAP))相容,与碱、胺及碱金属氰化物(如NaCN)不相容。CL-20的笼形结构使其具有一些优异的性能,这些性能(如燃烧热、爆速、爆压、氧平衡)在很多方面优于HMX,具体见表 2[20-23]。其中, ε-CL-20的性能最为优异,以圆筒试验及钽板实验测得的能量输出,ε-CL-20比HMX高约14%。预计CL-20在固体推进剂、混合炸药及发射药等技术领域具有广阔的应用前景,它的应用将会提升传统武器的性能。表 2显示,不同晶型CL-20的特性落高值大小顺序为ε->β->γ->α·H2O-,尽管α-CL-20的特性落高值较低,但不能肯定它的撞击感度就比其它晶型高,因为CL-20的撞击感度还与其粒度、粒度分布及晶体形貌(圆角还是棱角)有关。
CL-20是HMX的理想替代物,但它的机械感度略高于HMX,经过降感处理后方可满足安全使用的需求。影响CL-20感度的因素主要有化学纯度、所含杂质的性质、晶型纯度以及结晶质量,因此重结晶是降低CL-20感度、提高性能的有效方法。
3 CL-20的重结晶及晶型转变研究现状 3.1 CL-20重结晶的方法CL-20易溶解于含羰基的溶剂如丙酮、乙酸乙酯、N, N-二甲基甲酰胺(DMF)等; 在不含羰基的醇、醚、硝基烷烃中溶解度较小; 不溶于烃、卤代烃及水[24-25]。因此,可用于重结晶CL-20的方法有溶剂-非溶剂法、溶剂蒸发法; 但不适宜用降温法,因为CL-20在酯、酮等溶剂中的溶解度随温度变化不明显。
3.1.1 溶剂-非溶剂法溶剂-非溶剂法重结晶CL-20时,通常对CL-20的溶解度大于20%的溶剂可作为良溶剂,而小于5%的可作为非溶剂,并要求良溶剂与非溶剂易于混合、有较好的相容性。
常用的方法[6]是将CL-20溶于乙酸乙酯中,缓慢滴加非溶剂氯仿形成过饱和溶液,结晶得到ε-CL-20。该方法的重复性好,易得到目标晶型; 但制得的晶体缺陷多如孔隙、孪晶等,并且氯仿对环境的污染大,在与乙酸乙酯混合后难以分离,回收困难。
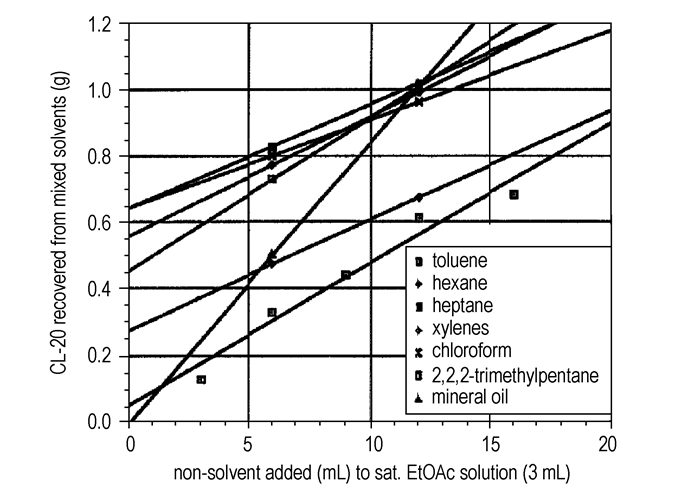
Johnston等[26]以乙酸乙酯为溶剂,选择无氯的非溶剂如烷烃、芳香烃等进行重结晶,考察了非溶剂加入量对CL-20晶体析出量的影响,结果如图 1所示。溶剂与非溶剂体积比一般为1:3~1:5,并且加入的非溶剂量越大,析出的ε-晶型晶体越多。选用己烷、氯仿等非溶剂得到的CL-20晶体量明显比用甲苯、二甲苯的多,这可能是由溶剂与非溶剂的互溶程度不同引起的。
|
图 1 非溶剂加入量与CL-20晶体析出量的关系[26] Fig.1 Relationship of non-solvent addition (mL) and the amount of CL-20 recovered |
使用重结晶提高ε-CL-20晶型纯度,可同时加入少量添加剂,以改善CL-20晶体质量。陈华雄等[27]使用溶剂-非溶剂法通过加入晶体生长控制剂(分子具有羟基或羧基或氨基,如马来酸、季戊四醇、氨基乙酸等)制得球形化(多面体形)ε-CL-20晶体,该晶体的撞击感度略有降低(特性落高值H50为26~52 cm),高效液相色谱测定化学纯度为98%~99%。
将超声与溶剂-非溶剂法结合,可制得细颗粒的CL-20晶体,以满足某些推进剂的高燃速要求[28]。但超声在改变CL-20晶体尺寸的同时,也影响了CL-20的晶型。Sivabalan等[29]在乙酸乙酯/正庚烷体系中,超声作用下重结晶CL-20。与无超声的方法对比,该方法制得的CL-20晶体具有钝感、颗粒小((5±1) μm)、尺寸分布窄的特点。但该研究人员并没有给出所制得的CL-20晶体的晶型,其晶体的形貌是类似菱形的薄片晶体。而据文献报道[30-33],ε-CL-20是纺锤形或多面体形的密实晶体,β-CL-20是针状或枫叶形的类片状晶体。因此单从晶体形貌判断,Sivabalan等制得的CL-20晶体很可能不是ε-晶型,而是β-晶型。
溶剂-非溶剂法重结晶CL-20安全可靠,已得到广泛应用,但混合溶剂的处理提高了成本。在溶剂体系中严格要求不能含水,否则将有α-CL-20形成,会降低CL-20的晶型纯度。
3.1.2 溶剂蒸发法溶剂蒸发法要求所使用的溶剂具有较高的蒸气压、容易挥发,用该方法重结晶CL-20时,一般以酯或酮为溶剂。但通常CL-20在这类溶剂中有很大的溶解度,如果再蒸发部分溶剂,CL-20溶液将变得粘稠,有可能导致晶体缺陷增多并发生团聚。为解决此问题,通常是再加入适量非溶剂或增塑剂等。
Lee等[34]以乙酸乙酯为溶剂研究了CL-20在25~70 ℃下蒸发结晶时晶体密度的变化情况发现,蒸发速率或CL-20起始浓度越大,晶体生长越快,形成的晶体孔隙也越多,导致ε-CL-20晶体密度降低; 而温度升高时,则阻碍了CL-20分子堆积,延缓了晶体生长,从而有利于提高晶体密度。在高蒸发速率和较高温度下重结晶CL-20时,趋向于得到β-晶型。说明通过控制动力学条件,可得到亚稳晶型晶体。
Bescond等[35]以酯或酮为溶剂溶解CL-20,加入芳香烃等非溶剂形成饱和溶液,再加入ε-CL-20晶种并将溶剂缓慢蒸发(要求溶剂的挥发性比非溶剂大)后,可获得10~100 μm的晶体。该方法晶体析出率高,但蒸发的溶剂易对环境造成污染。Snderson等[36]也采用了相同的方法,只是将非溶剂换成了硝酸酯(如硝化甘油、硝化三乙二醇,硝化丁三醇等),蒸发结晶后再用非溶剂冲洗,得到了形貌单一的ε-CL-20。
溶剂蒸发法工艺简单、易与其它重结晶方法联用; 但结晶点难以确定,晶体的尺寸也较难控制,因此较少采用该方法对CL-20进行重结晶,相关的文献报道也不多。此外,蒸发溶剂需要较高的温度,CL-20在重结晶时分解会加剧,导致晶体纯度不高。
3.2 CL-20晶型转变的理论解释使用上述方法重结晶CL-20时发现,通常最先形成的是亚稳晶型,而后再逐渐转变为稳定晶型,该现象与Ostwald规则相符合。1897年Wilhelm Ostwald发现处于热力学不稳定状态的体系,在向其稳定态过渡时,有时不是直接过渡到最稳定的状态(即自由能最低的状态),而是过渡到其自由能降低较小的中间状态,这一现象称为Ostwald规则[37](Ostwald′s rule of stages)。根据该规则,从热力学与动力学相结合角度,可解释CL-20的晶型转变过程[38]。
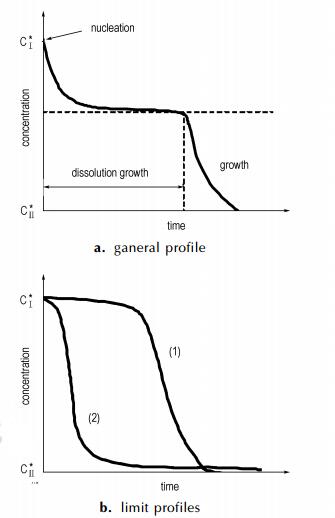
CL-20的重结晶过程包括一个溶液转晶过程。在热力学上,倾向于形成自由能最低、最稳定的ε-晶型; 但在动力学上,起始时亚稳晶核(如β-晶型)的形成及生长速率比ε-稳定晶型快得多,使得溶液中首先析出亚稳晶型并降到该晶型的饱和浓度。随着结晶的进行,ε-晶核开始长大导致溶液的浓度降低,使得亚稳态晶体逐渐溶解,而稳定态晶体不断生长,最终得到热力学上最稳定的ε-晶型。该过程称为溶剂介导相变[39-40](solvent-mediated phase transition,SMPT),可用图 2来表示。在不同的溶剂体系中,若稳定晶型的生长速率大于亚稳晶型的溶解速率,则为亚稳态溶解控制; 反之,则为稳定态生长控制。
|
图 2 溶液中晶型转变时浓度随时间变化情况[39] Fig.2 Concentration vs time during a polymorphic transition in solution CⅠ* and CⅡ* are the solubilities of the two phases, (a) general profile and (b) limit profiles; curve (1) transformation is controlled by growth of the stable form (Ⅱ) and curve (2) transformation is controlled by dissolution of the metastable form (Ⅰ) |
Kim等[41]将溶解了CL-20的乙酸乙酯快速倾入氯仿中,立即析出晶体,用FTIR表征确定为β-晶型,将该溶液继续搅拌结晶,而后得到ε-晶型。测得β-、ε-CL-20室温下在该溶剂体系中的溶解度为:Cβ->Cε-,确认ε-为稳定晶型而β-为亚稳晶型,该结果与Ostwald规则一致。若将β-晶型从溶液中滤出并置于室温空气中,则不会发生晶型转变。说明此晶型转变的机理是溶剂介导相变(SMPT)机理,晶型转变的驱动力是由β-和ε-晶型在溶剂中的溶解度差产生的,该差值越小时,β-晶型向ε-晶型转变的速率越慢。
用Ostwald规则和SMPT机理能较好地解释CL-20在重结晶时的晶型转变行为,但这只是定性描述。若能在动力学上定量确定CL-20的晶型转变速率,在热力学上准确测定CL-20晶型转变的吸热或放热量,则有助于研究CL-20晶型转变过程的机理和控制。
3.3 CL-20晶型转变的影响因素 3.3.1 溶剂溶剂是晶体生长的介质,溶剂与CL-20的相互作用决定了CL-20在溶液中的存在状态,并对CL-20晶体生长行为和晶型转变具有重要影响[42-43]。溶剂的极性、介电常数、质子化作用等是影响CL-20重结晶过程中晶型转变的内在因素。
金韶华等[44-45]认为溶剂的偶极矩对CL-20的晶型转变有重要影响,特别是对CL-20晶核形成有重要作用。常温下不加晶种时,以乙酸乙酯或丙酮为溶剂,采用偶极矩小的非溶剂如环己烷、甲苯等重结晶,均可使CL-20以ε-晶型析出; 反之,采用偶极矩大的非溶剂如水、乙醇、丙三醇、氯仿等重结晶,则以其它晶型析出。溶剂的偶极矩可归因于溶剂效应,较大偶极矩的溶剂,诱导CL-20晶核向非对称结构的α-或γ-晶型结晶; 而较小偶极矩的溶剂,则趋向于得到结构对称性较大的ε-晶型晶体。刘进全等[46-47]研究了ε-CL-20在不同偶极矩溶剂中,于70 ℃、80 ℃、90 ℃下的晶型稳定性,得出了相同的结论,小偶极矩溶剂有利于ε-晶型的稳定。
宋振伟等[48]将ε-CL-20置于不同溶剂中溶解,室温下自然挥发结晶,发现在丙酮、丙酮/乙醇(体积比1:1)、丙酮/CH2Cl2(体积比2:1)中转变为α-晶型,而在乙酸乙酯中转变为β-晶型。该研究人员认为溶解度小的溶剂对ε-晶型有稳定作用,混合溶剂体系中晶型转变与溶剂体积比有关,并且偶极矩小的溶剂有利于ε-晶型的形成。但是该研究人员仅从溶剂性质角度考虑晶型的变化,是不充分的。笔者认为得到的α-CL-20是由丙酮中含有杂质水导致的,若将溶剂中的水分除尽,则不会出现α-晶型; 而β-CL-20的出现可能与乙酸乙酯的挥发速率和结晶时间有关,若挥发越慢、结晶时间越长,则起始析出的β-晶型就会逐渐转变为ε-晶型。
因此,溶剂的性质在一定程度上影响了CL-20分子在溶液中的存在状态,但并不能单独作为控制晶型转变的依据。如果在某重结晶体系中,控制CL-20的浓度,恰好使ε-晶型是过饱和,而β-晶型是不饱和,则溶剂对这两种晶型的相对成核速率没有影响,溶液中只有ε-晶型析出,也就不会发生晶型转变。
此外,部分溶剂在重结晶时参与了CL-20晶体的形成,析出溶剂加合物晶体[49-50],如水、二甲亚砜、DMF、二氧六环、环丁砜、γ-丁内酯、六甲基磷酰三胺。这种溶剂加合物晶体一旦析出,在重结晶溶液中很难再发生晶型转变,以至于不能得到ε-CL-20晶体。故要得到晶型纯度较高的ε-CL-20晶体,应避免使用此类溶剂。
3.3.2 温度温度不仅影响CL-20在溶液中的过饱和度和晶体生长速率,还影响CL-20的稳定性[51]。升高温度,不同晶型CL-20晶体的Gibbs自由能变化程度不同,有可能使得原来稳定的晶型,在高于某温度点时变为亚稳晶型,从而改变晶型转变的路径[52-53]。
Foltz等[13-14]研究了ε-CL-20在甲苯、二甲苯等溶剂中加热时的晶型转变行为发现,温度越高,越有利于γ-晶型的形成。该研究人员认为ε-与γ-晶型存在相互转变临界温度为(64±1) ℃,高于64 ℃时,γ-CL-20由亚稳晶型变为稳定晶型,而ε-CL-20反之。Holtz等[24]在室温~74 ℃测定ε-CL-20于酯、醚、烃等溶剂中的溶解度时也发现了ε-晶型向γ-晶型转变的现象,说明γ-晶型的形成与温度有关。
然而,Hamilton等[54-55]结合溶剂-非溶剂法与溶剂蒸发法,将CL-20溶解于乙酸乙酯中,加入溶解度较低的溶剂(如甲酸苄酯、乙酸苄酯等)并滴加少量辅助非溶剂如环烷烃油或石蜡油,再将该饱和溶液加热到60 ℃以上(如71~94 ℃),并加入ε-晶种,缓慢蒸出乙酸乙酯,使得ε-CL-20晶体在非溶剂环境中析出。该法获得的ε-晶型的纯度较高,晶体密度为2.034~2.036 g·cm-3。
根据Foltz等的研究结果,Hamilton等制得的晶体应是γ-晶型,但却得到较好质量的ε-晶型。说明晶型转变临界温度还与CL-20所处的溶剂氛围有关。某些非溶剂与CL-20分子的作用,使得ε-晶型向γ-晶型转变的能垒升高或降低,导致ε-晶型的稳定温度范围发生改变。
不同晶型CL-20的形成与温度和溶剂性质有关,体现了CL-20晶型转变过程的复杂性。因此,对于不同的重结晶体系,晶型转变临界温度并不都是64 ℃,需将温度与溶剂等因素综合考虑,以准确控制CL-20的晶型转变路径。
3.3.3 其它因素重结晶时为了控制CL-20的晶型转变过程,除了考察溶剂和温度的影响,还要研究溶剂/非溶剂比例、非溶剂滴加速率、晶种、搅拌方式等因素的作用[56-58]。非溶剂量越大,CL-20在重结晶溶液中的溶解度越小,优先析出的亚稳晶型的再溶解以及稳定晶型的生长将变缓,从而影响晶型的转变速率。非溶剂滴加速率越快,CL-20溶液的过饱和度增加速率也越快,在动力学上越有利于获得亚稳晶型。加入晶种,可诱导CL-20晶体以目标晶型析出。若CL-20原料未完全溶解就进行重结晶,极有可能直接得到该原料晶型,而不是稳定的ε-CL-20。快速搅拌可加速溶质在溶液中的活动性,促使亚稳晶型的溶解,从而有利于稳定晶型的生长。因此,探索晶型转变与各因素的内在关系,寻求最佳的重结晶条件,可制得高晶型纯度、高结晶质量的ε-CL-20。
4 结论与展望CL-20是现有能量最高的单质炸药,具有多种晶型,在重结晶时不易得到单一晶型晶体。ε-CL-20中混入的α-、β-或γ-晶型,都会在一定程度上降低CL-20的密度、增加感度,限制CL-20的广泛使用。CL-20主要的重结晶方法有溶剂-非溶剂法、溶剂蒸发法,通过优化结晶工艺,选择合适的重结晶条件,可提高ε-CL-20晶型纯度、改善晶体质量、从而降低感度并提高性能。但CL-20晶型转变的影响因素较多、且具复杂性,溶剂、温度、过饱和度等都会影响CL-20的晶型转变行为。现有的文献报道都未能准确充分地阐述各因素对晶型转变的影响,并且对重结晶过程中的晶型转变路径还未见详细的研究。此外,CL-20重结晶时的晶型转变机理还不是很清楚。
因此,研究CL-20重结晶时的晶型转变行为,可从以下几个方面着手:(1)使用不同的溶剂体系重结晶CL-20,并结合温度等因素,考察晶型的转变过程; (2)使用Ostwald规则和SMPT机理解释晶型转变行为,并从热力学和动力学角度,定量地测定晶型转变时的热量变化和晶体生长速率; (3)从理论上模拟计算CL-20晶型转变的路径及能量变化,并与实验结果对比; (4)控制CL-20的晶型转变路径,制备晶型纯度较高的ε-CL-20晶体,并结合控制CL-20的形貌、改善晶体质量,从而降低CL-20感度并提高性能。
| [1] |
Bernstein J.
Polymorphism in Molecular Crystals[M]. Oxford: Oxford University Press, 2002: 275-296. |
| [2] |
欧育湘, 刘进全.
高能量密度化合物[M]. 北京: 国防工业出版社, 2005: 157-176.
OU Yu-xiang, LIU Jin-quan. High Energy Density Compounds[M]. Beijing: National Defence Industry Press, 2005: 157-176. |
| [3] |
Nair U R, Sivabalan R, Gore G M, et al. Hexantitrohexaazaisowurtzitane(CL-20) and CL-20-based formulations(review)[J].
Combustion, Explosion, and Shork Waves, 2005, 41(2): 121-132. DOI:10.1007/s10573-005-0014-2 |
| [4] |
曾贵玉, 聂福德, 刘晓东, 等. 六硝基六氮杂异伍兹烷(CL-20)的研究进展[J].
含能材料, 2000, 8(3): 130-134. ZENG Gui-yu, NIE Fu-de, LIU Xiao-dong, et al. The development of hexanitrohexaazaisowurtzitane[J]. Chinese Journal of Energetic Materials(Hanneng Cailiao), 2000, 8(3): 130-134. |
| [5] |
Hoffman D M. Voids and density distributions in 2, 4, 6, 8, 10, 12-hexanitro-2, 4, 6, 8, 10, 12-hexaazaisowurtzitane (CL-20) prepared under various conditions[J].
Propellants, Explosives, Pyrotechnics, 2003, 28(4): 194-200. DOI:10.1002/(ISSN)1521-4087 |
| [6] |
Nielsen A T. Caged polynitramine compound: US 5693794[P], 1997.
|
| [7] |
Nielsen A T, Chafin A P, Christian S L, et al. Synthesis of polyazapolycyclic caged polynitramines[J].
Tetrahedron, 1998, 54(39): 11793-11812. DOI:10.1016/S0040-4020(98)83040-8 |
| [8] |
欧育湘, 刘进全, 孟征, 等. 六硝基六氮杂异伍兹烷转晶工艺最新研究进展[J].
含能材料, 2005, 13(2): 124-127. OU Yu-xiang, LIU Jin-quan, MENG Zheng, et al. Recent development on crystal transition technology of hexanitrohexaazaisowurtzitane[J]. Chinese Journal of Energetic Materials(Hanneng Cailiao), 2005, 13(2): 124-127. |
| [9] |
Bellamy A J. A simple method for the purification of crude hexanitrohexaazaisowurtzitane (HNIW or CL-20)[J].
Propellants, Explosives, Pyrotechnics, 2003, 28(3): 145-152. DOI:10.1002/prep.200390021 |
| [10] |
Geetha M, Nair U R, Sarwade D B, et al. Studies on CL-20: The most powerful high energy material[J].
Journal of Thermal Analysis and Calorimetry, 2003, 73(3): 913-922. DOI:10.1023/A:1025859203860 |
| [11] |
Golovina N I, Utenyshev A N, Bozhenko K V, et al. The energy parameters of 2, 4, 6, 8, 10, 12-hexanitro-2, 4, 6, 8, 10, 12-hexaazaisowurtzitane polymorphs and their phase transitions[J].
Russian Journal of Physical Chemistry A, 2009, 83(7): 1153-1159. DOI:10.1134/S0036024409070188 |
| [12] |
Sikder A K, Sikder N. A review of advanced high performance, insensitive and thermally stable energetic materials emerging for military and space applications[J].
Journal of Hazardous Materials, 2004, 112(1): 1-15. |
| [13] |
Foltz M F, Coon C L, Garcia F, et al. The thermal stability of the polymorphs of hexanitrohexaazaisowurtzitane, Part Ⅰ[J].
Propellants, Explosives, Pyrotechnics, 1994, 19(1): 19-25. DOI:10.1002/(ISSN)1521-4087 |
| [14] |
Foltz M F, Coon C L, Garcia F, et al. The thermal stability of the polymorphs of hexanitrohexaazaisowurtzitane, Part Ⅱ[J].
Propellants, Explosives, Pyrotechnics, 1994, 19(3): 133-144. DOI:10.1002/(ISSN)1521-4087 |
| [15] |
Russell T P, Miller P J. High-pressure phase transition in γ-hexanitrohexaazaisowurtzitane[J].
The Journal of Physical Chemistry, 1992, 96(13): 5509-5512. DOI:10.1021/j100192a060 |
| [16] |
Millar D I A, Maynard-Casely H E, Kleppe A K, et al. Putting the squeeze on energetic materials-structural characterisation of a high-pressure phase of CL-20[J].
Crystal Enginning Common, 2010, 12(9): 2524-2527. DOI:10.1039/c002701d |
| [17] |
Bernstein J, Davey R J, Henck J O. Concomitant polymorphs[J].
Angewandte Chemie International Edition, 1999, 38(23): 3440-3461. DOI:10.1002/(SICI)1521-3773(19991203)38:23<>1.0.CO;2-U |
| [18] |
Kholod Y, Okovytyy S, Kuramshina G, et al. An analysis of stable forms of CL-20: A DFT study of conformational transitions, infrared and raman spectra[J].
Journal of Molecular Structure, 2007, 843: 14-25. DOI:10.1016/j.molstruc.2006.12.031 |
| [19] |
Sorescu D C, Rice B M, Thompson D L. Molecular packing and NPT-molecular dynamics investigation of the transferability of the RDX intermolecular potential to 2, 4, 6, 8, 10, 12-hexanitrohexaazaisowurtzitane[J].
The Journal of Physical Chemistry B, 1998, 102(6): 948-952. DOI:10.1021/jp973200e |
| [20] |
Simpson R L, Urtiew P A, Ornellas D L, et al. CL-20 performance exceeds that of HMX and its sensitivity is moderate[J].
Propellants, Explosives, Pyrotechnics, 1997, 22(5): 249-255. DOI:10.1002/(ISSN)1521-4087 |
| [21] |
陈鲁英, 杨培进, 张林军, 等. CL-20炸药性能研究[J].
火炸药学报, 2003, 26(3): 65-67. CHEN Lu-ying, YANG Jin-pei, ZHANG Lin-jun, et al. Study of the performance of explosive CL-20[J]. Chinese Journal of Explosives & Propellants, 2003, 26(3): 65-67. |
| [22] |
LI Ming, TAN Wu-jun, KANG Bin, et al. The elastic modulus of β-HMX crystals determined by nanoindentation[J].
Propellants, Explosives, Pyrotechnics, 2010, 35(4): 379-383. DOI:10.1002/prep.201000018 |
| [23] |
欧育湘, 王才, 潘则林, 等. 六硝基六氮杂异伍兹烷的感度[J].
含能材料, 1999, 7(3): 100-102. OU Yu-xiang, WANG Cai, PAN Ze-lin, et al. Sensitivity of hexanitrohexazaisowurtzitane[J]. Chinese Journal of Energetic Materials(Hanneng Cailiao), 1999, 7(3): 100-102. |
| [24] |
Holtz E V, Donald O, Foltz M F, et al. The solubility of ε-CL-20 in selected materials[J].
Propellants, Explosives, Pyrotechnics, 1994, 19(4): 206-212. DOI:10.1002/(ISSN)1521-4087 |
| [25] |
Torry S, Cunliffi A. Polymorphism and solubility of CL-20 in plasticisers and polymers[C]//31st Int Annual Conf of ICT. Karlsruhe, 2000: 107/101-107/112.
|
| [26] |
Johnston H E, Dickson, Tennant, et al. Process of crystalling 2, 4, 6, 8, 10, 12-hexanitro-2, 4, 6, 8, 10, 12-hexaazatetracyclo[5. 5. 0. 0. 5, 903, 11]-dodecane: US 5874574[P], 1999.
|
| [27] |
陈华雄, 阵树森, 刘进全, 等. 一种球形化的六硝基六氮杂异伍兹烷晶体及其制备方法: CN, 101624394A[P], 2009.
CHEN Hua-xiong, CHEN Shu-sen, LIU Jin-quan, et al. Sphericized hexanitrohexaazaisowurtzitane crystal and preparation method: CN, 101624394A[P], 2009. |
| [28] |
Patil M N, Gore G M, Pandit A B. Ultrasonically controlled particle size distribution of explosives: A safe method[J].
Ultrasonics Sonochemistry, 2008, 15(3): 177-187. DOI:10.1016/j.ultsonch.2007.03.011 |
| [29] |
Sivabalan R, Gore G M, Nair U R, et al. Study on ultrasound assisted precipitation of CL-20 and its effect on morphology and sensitivity[J].
Journal of Hazardous Materials, 2007, 139: 199-203. DOI:10.1016/j.jhazmat.2006.06.027 |
| [30] |
ThomeV, KemP B, Herrmann M. Solvent effects on the morphology of epslion-CL-20 crystals[C]//32nd Int Annual Conf of ICT. Karlsruhe, 2001: 157/1-157/7.
|
| [31] |
Benazet S, Jacob G. Crystal engineering of HNIW by molecular modeling using Genmol[C]//33th Int Annual Conf of ICT. Karlsruhe, 2002: 29/1-29/8.
|
| [32] |
Thome V, Herrmann M. Determination of the morphology of HNIW-phases by the attachment energy method[C]//34th Int Annual Conf of ICT. Karlsruhe, 2003: 102/1-102/12.
|
| [33] |
孟征, 卫宏远. 晶形控制剂对ε-HNIW晶体形貌的影响[J].
含能材料, 2011, 19(2): 165-169. MENG Zheng, WEI Hong-yuan. Effent of crystal modifier on crystal morphology of ε-HNIW[J]. Chinese Journal of Energetic Materials(Hanneng Cailiao), 2011, 19(2): 165-169. |
| [34] |
Lee M H, Kim J H, Park Y C, et al. Control of crystal density of ε-hexanitrohexaazaisowurzitane in evaporation crystallization[J].
Industrial&Engineering Chemistry Research, 2007, 46(5): 1500-1504. |
| [35] |
Bescond P. Process for producing the epsilon polymorphic form of hexanitrohexaazaisowurtzitane: US 5973149[P], 1999.
|
| [36] |
Sanderson A J, Hamilton R S, Warner K F. Crystallization of 2, 4, 6, 8, 10, 12-hexanitro-2, 4, 6, 8, 10, 12-hexaazatetracyclo[5. 5. 0. 0. 5, 903, 11]-dodecane: US 6350871B1[P], 2002.
|
| [37] |
Ostwald W. Studien über die bildung und umwandlung fester körper[J].
Zeitschrift für Physikalische Chemie, 1897, 22: 289-330. |
| [38] |
Threlfall T. Structural and thermodynamic explanations of ostwald's rule[J].
Organic Process Research & Development, 2003, 7(6): 1017-1027. |
| [39] |
Mangin D, Puel F, Veesler S. Polymorphism in processes of crystallization in solution: A practical review[J].
Organic Process Research & Development, 2009, 13(6): 1241-1253. |
| [40] |
Croker D, Hodnett B K. Mechanistic features of polymorphic transformations: The role of surfaces[J].
Crystal Growth & Design, 2010, 10(6): 2806-2816. |
| [41] |
Kim J H, Park Y C, Yim Y J, et al. Crystallization behavior of hexanitrohexaazaisowurtzitane at 298 K and quantitative analysis of mixtures of its polymorphs by FTIR[J].
Journal of Chemical Engineering of Japan, 1998, 31(3): 478-481. DOI:10.1252/jcej.31.478 |
| [42] |
Khoshkho S, Anwar J. Crystallization of polymorphs: The effect of solvent[J].
Journal of Physics D: Appliced Physics, 1993, 26(8B): B90-B93. DOI:10.1088/0022-3727/26/8B/013 |
| [43] |
Threlfall T. Crystallisation of Polymorphs: Thermodynamic insight into the role of solvent[J].
Organic Process Research & Development, 2000, 4(5): 384-390. |
| [44] |
JIN Shao-hua, YU Zhang-xing, SONG Quan-cai, et al. The role of physical properties of solvents in the preparation of HNIW[C]//34th Int Annual Conf of ICT. Karlsruhe, 2003: 57/51-57/55.
|
| [45] |
金韶华, 雷向东, 欧育湘, 等. 溶剂性质对六硝基六氮杂异伍兹烷晶型的作用[J].
兵工学报, 2005, 26(6): 743-745. JIN Shao-hua, LEI Xiang-dong, OU Yu-xiang, et al. Influence of anti-solvent property on the modes of crystallization of HNIW[J]. Acta Armamentarii, 2005, 26(6): 743-745. |
| [46] |
刘进全, 欧育湘, 金韶华, 等. 溶剂及温度对ε-HNIW晶型及热安定性的影响[J].
火炸药学报, 2005, 28(2): 56-59. LIU Jin-quan, OU Yu-xiang, JIN Shao-hua, et al. The influences of solvents and temperature on polymorphs and thermal stability of ε-HNIW[J]. Chinese Journal of Explosives & Propellants, 2005, 28(2): 56-59. |
| [47] |
刘进全, 欧育湘, 孟征, 等. ε-HNIW在不同溶剂中的晶型稳定性[J].
含能材料, 2006, 14(2): 108-110. LIU Jin-quan, OU Yu-xiang, MENG Zheng, et al. Polymorph stability of ε-HNIW in different solvents[J]. Chinese Journal of Energetic Materials(Hanneng Cailiao), 2006, 14(2): 108-110. |
| [48] |
宋振伟, 严启龙, 李笑飞, 等. 溶剂中ε-CL-20的晶型变化[J].
含能材料, 2010, 18(6): 648-653. SONG Zhen-wei, YAN Qi-long, LI Xiao-fei, et al. Crystal transition of ε-CL-20 in different solvent[J]. Chinese Journal of Energetic Materials(Hanneng Cailiao), 2010, 18(6): 648-653. |
| [49] |
赵信岐, 刘娟. 六硝基六氮杂异伍兹烷的分子络合物[J].
北京理工大学学报, 1996, 16(5): 494-497. ZHAO Xin-qi, LIU Juan. Some molecular complexes of hexanitrohexaazaisowurtzitane[J]. Journal of Beijing Institute of Technology, 1996, 16(5): 494-497. |
| [50] |
金韶华, 陈树森, 雷向东. HNIW与二甲基甲酰胺、二甲基亚砜分子加合物的研究[J].
兵工学报, 2008, 29(1): 90-93. JIN Shao-hua, CHEN Shu-sen, LEI Xiang-dong. Investigation of adducts of HNIW with DMF and DMSO[J]. Acta Armamentarii, 2008, 29(1): 90-93. |
| [51] |
Sato K. Polymorphic transformations in crystal growth[J].
Journal Physics D: Applied physics, 1993, 26: B77-B84. DOI:10.1088/0022-3727/26/8B/011 |
| [52] |
Chukanov N V, Golovina N I, Nedelko V V, et al. Phase transformation hexanitrohexaazaisowurtzitane[C]//32nd Int Annual Conf of ICT. Karlsruhe, 2001: 107/101-107/109.
|
| [53] |
Chukanov N V, Korwounskii B L, Nedelko V V, et al. Kinetic of dehydration and phase transitions in hexanitrohexaazaisowurtzitane: Effect of particle sizes[C]//37th Int Annual Conf of ICT. Karlsruhe, 2006: 29/21-29/12.
|
| [54] |
Hamilton R S. Crystallization of 2, 4, 6, 8, 10, 12-hexanitro-2, 4, 6, 8, 10, 12-hexaazatetracyclo[5. 5. 0. 0. 5, 903, 11]-dodecane: US 0130503[P], 2003.
|
| [55] |
Hamilton R S. High temperature crystallization of 2, 4, 6, 8, 10, 12-hexanitro-2, 4, 6, 8, 10, 12-hexaazatetracyclo[5. 5. 0. 0. 5, 903, 11]-dodecane: US 7288648[P], 2007.
|
| [56] |
Lapina Y T, Savitskii A S, Motina E V, et al. Polymorphic transformations of hexanitrohexaazaisowurtzitane[J].
Russian Journal of Applied Chemistry, 2009, 82(10): 1821-1828. DOI:10.1134/S1070427209100140 |
| [57] |
Kitamura M. Controlling factor of polymorphism in crystallization process[J].
Journal of Crystal Growth, 2002, 237(239): 2205-2214. |
| [58] |
Llinas A, Goodman J M. Polymorph control: Past, present and future[J].
Drug Discovery Today, 2008, 13(5): 198-210. |
The phenomenon of polymorphic transformation in CL-20 recrystallization was introduced. It can be explained by Ostwald′s rule of stages and may provide some academic guide for restraining the progress of polymorphic transformation to obtain the pure polymorphic crystal of α-, β-, γ-, ε-CL-20.